Exubera til behandling af diabetes
Mærkenavn: Exubera
Generisk navn: humant insulin
Doseringsform: inhalationspulver
Indhold:
Beskrivelse
Klinisk farmakologi
Kliniske studier
Indikationer og anvendelse
Kontraindikationer
Advarsler
Forholdsregler
Lægemiddelinteraktioner
Bivirkninger
overdosering
Dosering og administration
Hvordan leveres
Exubera, humant insulin [rDNA-oprindelse] Patientinformation (på almindeligt engelsk)
Beskrivelse
Exubera® består af blemmer, der indeholder humant insulininhalationspulver, der administreres ved hjælp af Exubera® Inhaler. Exubera-blister indeholder humant insulin produceret ved rekombinant DNA-teknologi under anvendelse af en ikke-patogen laboratoriestamme af Escherichia coli (K12). Kemisk set har humant insulin den empiriske formel C257H383N65O77S6 og en molekylvægt på 5808. Human insulin har følgende primære aminosyresekvens:
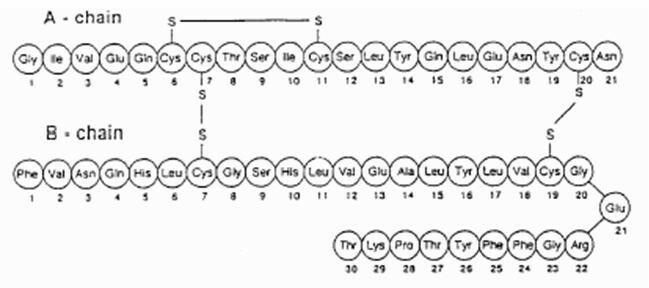
Exubera (humant insulin [rDNA-oprindelse]) Inhalationspulver er et hvidt til off-white pulver i en enhedsdosis blister (fyldmasse, se tabel 1). Hver enhedsdosisblister af Exubera indeholder en 1 mg eller 3 mg dosis insulin (se tabel 1) i a homogen pulverformulering indeholdende natriumcitrat (dihydrat), mannitol, glycin og natrium hydroxid. Når en Exubera-blister er indsat i inhalatoren, pumper patienten håndtaget på inhalatoren og trykker derefter på en knap, hvilket får blæren til at blive gennemboret. Insulininhalationspulveret spredes derefter ind i kammeret, så patienten kan inhalerer det aerosoliserede pulver.
Under standardiserede in vitro-testbetingelser leverer Exubera en specifik udsendt dosis insulin fra mundstykket til inhalatoren (se tabel 1). En brøkdel af den samlede partikelmasse udsendes som fine partikler, der er i stand til at nå den dybe lunge. Op til 45% af indholdet af blister på 1 mg og op til 25% af indholdet af blister kan holdes i blisterpakningen.
Tabel 1: Dosisnomenklatur og information
| Fyld masse (mg pulver) |
Nominel dosis (mg insulin) |
Emission Dose*,†(mg insulin) |
Fin partikeldosisc,†(mg insulin) |
|---|---|---|---|
| |||
| 1.7 | 1.0 | 0.53 | 0.4 |
| 5.1 | 3.0 | 2.03 | 1.0 |
Den faktiske mængde insulin, der leveres til lungen, afhænger af individuelle patientfaktorer, såsom inspirerende flowprofil. In vitro påvirkes ikke-udsendte aerosolmetrik ved strømningshastigheder over 10 L / min.
top
Klinisk farmakologi
Handlingsmekanisme
Den primære aktivitet af insulin er regulering af glukosemetabolisme. Insulin sænker blodglukosekoncentrationerne ved at stimulere perifer glukoseoptagelse af knoglemuskler og fedt og ved at hæmme glukoseproduktion i leveren. Insulin hæmmer lipolyse i adipocytten, inhiberer proteolyse og forbedrer proteinsyntesen.
Farmakokinetik
absorption
Exubera leverer insulin ved oral inhalation. Insulinet absorberes så hurtigt som subkutant administreret hurtigvirkende insulinanaloger og hurtigere end subkutant administreret regelmæssigt humant insulin hos raske individer og hos patienter med type 1 eller type 2 diabetes (se Figur 1).
Figur 1: Gennemsnitlige ændringer i fri insulinserumkoncentration (µU / ml) hos patienter med følgende type 2-diabetes Administration af enkeltdoser af inhaleret insulin fra Exubera (6 mg) og subkutant regelmæssigt humant insulin (18U)
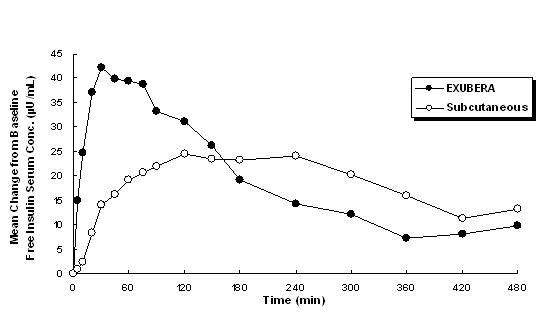
I kliniske studier på patienter med type 1 og type 2 diabetes nåede seruminsulin hurtigere end inhalation af Exubera end efter subkutan injektion af almindeligt humant insulin, 49 minutter (område fra 30 til 90 minutter) sammenlignet med 105 minutter (område fra 60 til 240 minutter), henholdsvis.
I kliniske studier faldt absorptionen af subkutant regelmæssigt humant insulin med stigende patientkropsmasseindeks (BMI). Absorptionen af insulin efter inhalation af Exubera var imidlertid uafhængig af BMI.
I en undersøgelse med raske forsøgspersoner blev systemisk insulineksponering (AUC og Cmax) efter administration af Exubera steg med en dosis i området fra 1 til 6 mg, når det blev administreret som kombinationer af 1 og 3 mg blærer.
I en undersøgelse, hvor doseringsformen af tre 1 mg blister blev sammenlignet med en 3 mg blister, Cmax og AUC efter administration af tre 1 mg blister var henholdsvis ca. 30% og 40% større end efter administration af en 3 mg blister (se DOSERING OG ADMINISTRATION).
Distribution og eliminering
Da rekombinant humant insulin er identisk med endogent insulin, forventes den systemiske distribution og eliminering at være den samme. Dette er dog ikke bekræftet for Exubera.
farmakodynamik
Exubera har som subkutant administreret hurtigvirkende insulinanaloger en hurtigere begyndelse af glukosesænkende aktivitet end subkutant administreret almindeligt humant insulin. Hos raske frivillige var varigheden af glukosesænkende aktivitet for Exubera sammenlignelig med subkutant administreret regelmæssigt humant insulin og længere end subkutant administreret hurtigvirkende insulinanaloger (se Figur 2).
Figur 2. Gennemsnitlig glukoseinfusionshastighed (GIR) Normaliseret til GIRmax for hvert emne Behandling versus tid hos sunde frivillige
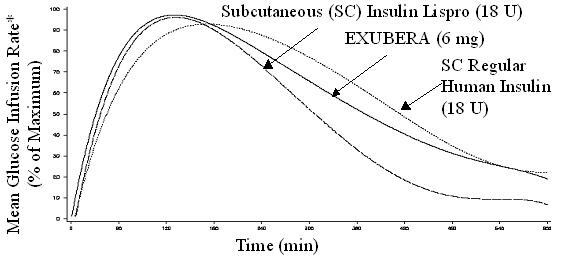
* Bestemmes som mængde glukose tilført for at opretholde konstante plasmaglucosekoncentrationer, normaliseret til maksimale værdier (procent af maksimale værdier); indikerer insulinaktivitet.
Når Exubera inhaleres, forekommer indtræden af glukosesænkende aktivitet hos raske frivillige inden for 10-20 minutter. Den maksimale effekt på glukosesænkning udøves cirka 2 timer efter indånding. Varigheden af glukosesænkende aktivitet er cirka 6 timer.
Hos patienter med type 1 eller type 2 diabetes har Exubera en større glukosesænkende virkning inden for de første to timer efter dosering sammenlignet med subkutant indgivet almindeligt humant insulin.
Den intra-individuelle variation af glukosesænkende aktivitet af Exubera er generelt sammenlignelig med den for subkutant administreret regelmæssigt humant insulin hos patienter med type 1 og 2-diabetes.
Særlige befolkninger
Pædiatriske patienter
Hos børn (6-11 år) og unge (12-17 år) med diabetes type 1 var tid til at maksimere insulinkoncentrationen for Exubera opnået hurtigere end for subkutan almindelig humaninsulin, hvilket er i overensstemmelse med observationer hos voksne patienter med type 1 diabetes.
Geriatriske patienter
Der er ingen åbenlyse forskelle i de farmakokinetiske egenskaber ved Exubera, når man sammenligner patienter over 65 år og yngre voksne patienter.
Køn
Hos personer med og uden diabetes blev der ikke observeret nogen tydelige forskelle i de farmakokinetiske egenskaber ved Exubera mellem mænd og kvinder.
Race
En undersøgelse blev udført i 25 raske kaukasiske og japanske ikke-diabetiske personer for at sammenligne farmakokinetiske og farmakodynamiske egenskaber ved Exubera mod subkutan injektion af almindeligt menneske insulin. De farmakokinetiske og farmakodynamiske egenskaber af Exubera var sammenlignelige mellem de to populationer.
Fedme
Absorptionen af Exubera er uafhængig af patientens BMI.
Nedsat nyrefunktion
Effekten af nedsat nyrefunktion på farmakokinetikken af Exubera er ikke undersøgt. Omhyggelig glukoseovervågning og dosisjustering af insulin kan være nødvendig hos patienter med nedsat nyrefunktion (se FORHOLDSREGLER, Nedsat nyrefunktion).
Nedsat leverfunktion
Effekten af nedsat leverfunktion på farmakokinetikken af Exubera er ikke undersøgt. Omhyggelig glukoseovervågning og dosisjustering af insulin kan være nødvendig hos patienter med leverdysfunktion (se FORHOLDSREGLER).
Graviditet
Absorptionen af Exubera hos gravide patienter med drægtigheds- og præ-gestation type 2-diabetes var i overensstemmelse med den hos ikke-gravide patienter med type 2-diabetes (se FORHOLDSREGLER).
Rygning
Hos rygere forventes den systemiske insulineksponering for Exubera at være 2 til 5 gange højere end hos ikke-rygere. Exubera er kontraindiceret til patienter, der ryger, eller som har ophørt med at ryge mindre end 6 måneder, før Exubera-behandlingen påbegyndes. Hvis en patient begynder eller fortsætter med at ryge, skal Exubera seponeres straks på grund af den øgede risiko for hypoglykæmi, og en alternativ behandling skal anvendes (se KONTRAINDIKATIONER).
I kliniske studier af Exubera hos 123 patienter (hvoraf 69 var rygere), oplevede rygere en hurtigere begyndelse af glukosesænkende virkning, større maksimal effekt og en større total glukosesænkende effekt (især i de første 2-3 timer efter dosering) sammenlignet med ikke-rygere.
Passiv cigaretrøg
I modsætning til stigningen i insulineksponering efter aktiv rygning, da Exubera blev administreret til 30 raske ikke-ryger-frivillige efter 2 timers eksponering for passiv cigaretrøg i en kontrolleret eksperimentel indstilling, insulin AUC og Cmax blev reduceret med ca. 20% og 30%, henholdsvis. Farmakokinetikken for Exubera er ikke undersøgt hos ikke-rygerne, der kronisk udsættes for passiv cigaretrøg.
Patienter med underliggende lungesygdomme
Brug af Exubera til patienter med underliggende lungesygdom, såsom astma eller KOL, anbefales ikke, fordi sikkerheden og effekten af Exubera i denne population ikke er blevet fastlagt (se ADVARSLER). Brug af Exubera er kontraindiceret til patienter med ustabil eller dårligt kontrolleret lungesygdom på grund af bred variationer i lungefunktion, der kan påvirke absorptionen af Exubera og øge risikoen for hypoglykæmi eller hyperglykæmi (se KONTRAINDIKATIONER).
I en farmakokinetisk undersøgelse hos 24 ikke-diabetiske personer med mild astma blev absorptionen af insulin efter administration af Exubera var i fravær af behandling med en bronchodilator ca. 20% lavere end absorptionen hos personer uden astma. I en undersøgelse blandt 24 ikke-diabetiske personer med kronisk obstruktiv lungesygdom (KOL) var det systemiske eksponering efter administration af Exubera var cirka to gange højere end hos normale personer uden KOLS (se FORHOLDSREGLER).
Indgivelse af albuterol 30 minutter før administration af Exubera hos ikke-diabetiske personer med både mild astma (n = 36) og moderat astma (n = 31) resulterede i en gennemsnitlig stigning i insulin AUC og Cmax på mellem 25 og 50% sammenlignet med når Exubera blev indgivet alene (se FORHOLDSREGLER).
top
Kliniske studier
Sikkerheden og effekten af Exubera er undersøgt hos ca. 2500 voksne patienter med type 1 og type 2 diabetes. Den primære effektivitetsparameter for de fleste undersøgelser var glykæmisk kontrol, målt ved reduktionen fra basislinien i hæmoglobin A1c (HbA1c).
Type 1 Diabetes
En 24-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse A) blev udført hos patienter med type 1-diabetes for at vurdere sikkerheden og effektiviteten af Exubera indgives før måltid tre gange dagligt (TID) med en enkelt natinjektion af Humulin® U Ultralente® (human insulinudvidet zinksuspension) (n = 136). Sammenligningsbehandlingen blev subkutant regelmæssigt humant insulin indgivet to gange dagligt (BID) (før morgenmad og før middag) med BID-injektion af NPH humant insulin (human insulin isophansuspension) (n = 132). I denne undersøgelse var middelalderen 38,2 år (interval: 20-64), og 52% af forsøgspersoner var mandlige.
En anden 24-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse B) blev udført hos patienter med type 1-diabetes for at vurdere sikkerhed og virkning af Exubera (n = 103) sammenlignet med subkutant almindeligt humant insulin (n = 103), når det blev administreret TID før måltider. I begge behandlingsarme blev NPH human insulin administreret BID (om morgenen og ved sengetid) som basalinsulin. I denne undersøgelse var middelalderen 38,4 år (interval: 19-65), og 54% af forsøgspersoner var mandlige.
I hver undersøgelse var reduktionen i HbA1c og antallet af hypoglykæmi sammenlignelige for de to behandlingsgrupper. Exubera-behandlede patienter havde en større reduktion i fastende plasmaglukose end patienter i sammenligningsgruppen. Procentdelen af patienter, der når et HbA1c-niveau på <8% (pr. Behandling af American Diabetes Association) Niveau på undersøgelsestidspunktet) og et HbA1c-niveau på <7% var sammenlignelige mellem de to behandlingsgrupper. Resultaterne for undersøgelser A og B er vist i tabel 2.
Tabel 2: Resultater af to 24-ugers, aktiv-kontrol, open-label forsøg hos patienter med type 1-diabetes (undersøgelser A og B)
| Undersøgelse A | Undersøgelse B | |||
|---|---|---|---|---|
| Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) | Exubera (TID) + NPH (BID) | SC R (TID) + NPH (BID) | |
| Prøvestørrelse | 136 | 132 | 103 | 103 |
| UL = Humulin® U Ultralente®; SC R = subkutant almindeligt humant insulin | ||||
| ||||
| HbA1c (%) | ||||
| Baseline middelværdi | 7.9 | 8.0 | 7.8 | 7.8 |
| Adj. gennemsnitlig ændring fra baseline | -0.2 | -0.4 | -0.3 | -0.2 |
| Exubera minus SC R* | 0.14 | -0.11 | ||
| 95% CI for behandlingsforskel | (-0.03, 0.32) | (-0.30, 0.08) | ||
| Fastende plasma-glukose (mg / dL) | ||||
| Baseline middelværdi | 191 | 198 | 178 | 191 |
| Adj. gennemsnitlig ændring fra baseline | -32 | -6 | -23 | 13 |
| Exubera minus SC R | -27 | -35 | ||
| 95% CI for behandlingsforskel | (-47, -6) | (-58, -13) | ||
| 2-timers postprandial glukosekoncentration (mg / dL) | ||||
| Baseline middelværdi | 283 | 305 | 273 | 293 |
| Adj. gennemsnitlig ændring fra baseline | -21 | 14 | -1 | -3 |
| Exubera minus SC R | -35 | 2 | ||
| 95% CI for behandlingsforskel | (-61, -8) | (-29, 32) | ||
| Patienter med slutningen af undersøgelsen HbA1c < 8%†| 64.0% | 68.2% | 74.8% | 66.0% |
| Patienter med slutningen af undersøgelsen HbA1c < 7% | 16.9% | 19.7% | 28.2% | 30.1% |
| Kropsvægt | ||||
| Baseline middelværdi (kg) | 77.4 | 76.4 | 76.0 | 76.9 |
| Adj. gennemsnitlig ændring fra baseline (kg) | 0.4 | 1.1 | 0.4 | 0.6 |
| Exubera minus SC R | -0.72 | -0.24 | ||
| 95% CI for behandlingsforskel | (-1.48, 0.04) | (-1.07, 0.59) | ||
| Slut på studiens daglige insulindosis | ||||
| Kortvirkende insulin | 13,4 mgc | 18.3 IE | 10,9 mgc | 25,7 IE |
| Langtidsvirkende insulin | 26,4 IE | 37,1 IE | 31,5 IE | 31,9 IE |
Type 2 Diabetes
Monoterapi hos patienter, der ikke er optimalt kontrolleret med diæt og træningsbehandling
En 12-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse C) blev udført hos patienter med type 2-diabetes ikke optimalt kontrolleret med diæt og motion, vurderer sikkerheden og effektiviteten af TID Exubera før måltid (n = 75) sammenlignet med en insulin-sensibiliserende middel. I denne undersøgelse var middelalderen 53,7 år (interval: 28-80), 55% af forsøgspersoner var mandlige, og det gennemsnitlige kropsmasseindeks var 32,3 kg / m2.
Efter 12 uger, HbA1c niveauer hos patienter behandlet med Exubera faldt 2,2% (SD = 1,0) fra en basislinje på 9,5% (SD = 1,1). Andelen af patienter, der blev behandlet med Exubera, når en afsluttende undersøgelse af HbA1c niveau på <8% steg til 82,7%. Andelen af patienter, der blev behandlet med Exubera, når en afsluttende undersøgelse af HbA1c niveau af
Monoterapi og tillægsbehandling hos patienter, der tidligere blev behandlet med oral middelterapi
En 12-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse D) blev udført hos patienter med type 2 diabetes, der i øjeblikket modtog behandling, men var dårligt kontrolleret, med to orale stoffer (OA). Baseline OA'er inkluderede en insulinsekretagoge og enten metformin eller en thiazolidinedion. Patienterne blev randomiseret til en af tre arme: fortsat OA-terapi alene (n = 96), skiftede til før måltid TID Exubera monoterapi (n = 102) eller tilføjelse af TID Exubera før måltid til fortsat OA-terapi (n = 100). I denne undersøgelse var middelalderen 57,4 år (interval: 33-80), 66% af forsøgspersoner var mandlige, og det gennemsnitlige kropsmasseindeks var 30 kg / m2.
Exubera monoterapi og Exubera i kombination med OA-terapi var bedre end OA-terapi alene til reduktion af HbA1c niveauer fra baseline. Hastighedsniveauerne for hypoglykæmi for de to Exubera-behandlingsgrupper var lidt højere end i gruppen med OA-terapi alene. Sammenlignet med OA-behandling alene er procentdelen af patienter, der når en HbA1c niveau på <8% (pr. behandling af American Diabetes Association-handlingsniveau på tidspunktet for undersøgelsens gennemførelse) og en HbA1c niveauet <7% var højere for patienter behandlet med Exubera monoterapi og Exubera i kombination med OA-terapi. Patienter i begge Exubera-behandlingsgrupper havde større reduktioner i fastende plasmaglukose end patienter, der blev behandlet med OA-behandling alene. Resultaterne for undersøgelse D er vist i tabel 3.
Tabel 3: Resultater af en 12-ugers aktiv-kontrol, open-label-undersøgelse hos patienter med type 2-diabetes, der ikke blev kontrolleret optimalt med dobbelt oral oral terapi (undersøgelse D)
| Undersøgelse D | Exubera monoterapi | OAs* | Exubera + OA'er |
|---|---|---|---|
| Prøvestørrelse | 102 | 96 | 100 |
| |||
| HbA1c (%) | |||
| Baseline middelværdi | 9.3 | 9.3 | 9.2 |
| Adj. gennemsnitlig ændring fra baseline | -1.4 | -0.2 | -1.9 |
| Exubera-gruppe minus OA'er†| -1.18†,c, § | -1.67†, ¶, § | |
| 95% CI for behandlingsforskel | (-1.41, -0.95) | (-1.90, -1.44) | |
| Fastende plasma-glukose (mg / dL) | |||
| Baseline middelværdi | 203 | 203 | 195 |
| Adj. gennemsnitlig ændring fra baseline | -23 | 1 | -53 |
| Exubera-gruppe minus OA'er | -24c | -53 ¶ | |
| 95% CI for behandlingsforskel | (-36, -11) | (-66, -41) | |
| Patienter med slutningen af undersøgelsen HbA1c < 8%# | 55.9% | 18.8% | 86.0% |
| Patienter med slutningen af undersøgelsen HbA1c < 7% | 16.7% | 1.0% | 32.0% |
| Kropsvægt | |||
| Baseline middelværdi (kg) | 89.5 | 88.0 | 88.6 |
| Adj. gennemsnitlig ændring fra baseline (kg) | 2.8 | 0.0 | 2.7 |
| Exubera-gruppe minus OA'er | 2.80c | 2.75 ¶ | |
| 95% CI for behandlingsforskel | (1.94, 3.65) | (1.89, 3.61) |
En 24-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse E) blev udført hos patienter med type 2-diabetes, der i øjeblikket modtog sulfonylurinstofterapi. Denne undersøgelse var designet til at vurdere sikkerheden og effektiviteten af tilsætningen af Exubera før måltid til fortsat sulfonylurinstofterapi (n = 214) sammenlignet med tilsætningen af metformin før måltid til fortsat sulfonylurinstofterapi (n = 196). Personer blev lagdelt i henhold til deres HbA1c i uge -1. To lag blev defineret: et lavt HbA1c-lag (HbA1c â € ¥ 8% til â ‰ ¤9,5%) og en høj HbA1c stratum (HbA1c > 9,5 til â ‰ ¤12%).
Exubera i kombination med sulfonylurinstof var bedre end metformin og sulfonylurinstof ved reduktion af HbA1c-værdier fra basislinien i gruppen med højt stratum. Exubera i kombination med sulfonylurinstof var sammenlignelig med metformin i kombination med sulfonylurinstof ved reduktion af HbA1c-værdier fra basislinien i gruppen med lavt stratum. Hastigheden af hypoglykæmi var højere efter tilsætningen af Exubera til sulfonylurinstof end efter tilsætningen af metformin til sulfonylurinstof. Procentdelen af patienter, der nåede mål HbA1c-værdier på 8% og 7%, var sammenlignelig mellem behandlingsgrupper i begge lag, ligesom reduktion i fastende plasmaglucose var ( Tabel 4).
En anden 24-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse F) blev udført hos patienter med type 2-diabetes, som i øjeblikket modtog metforminbehandling. Denne undersøgelse var designet til at vurdere sikkerheden og effektiviteten af tilsætningen af Exubera før måltid til fortsat metforminbehandling (n = 234) sammenlignet med tilsætningen af glibenclamid før måltid til fortsat metforminbehandling (n = 222). Personer i denne undersøgelse blev også lagdelt til et af to lag som defineret i undersøgelse E.
Exubera i kombination med metformin var bedre end glibenclamid og metformin til reduktion af HbA1c værdier fra baseline og opnåelse af mål HbA1c værdier i gruppen med højt stratum. Exubera i kombination med metformin var sammenlignelig med glibenclamid i kombination med metformin til reduktion af HbA1c værdier fra baseline og opnåelse af mål HbA1c værdier i gruppen med lavt stratum. Hastigheden af hypoglykæmi var lidt højere efter tilsætningen af Exubera til metformin end efter tilsætningen af glibenclamid til metformin. Reduktion i fastende plasmaglukose var sammenlignelig mellem behandlingsgrupper (se Tabel 4).
Tabel 4: Resultater af to 24-ugers, aktiv-kontrol, open-label-forsøg hos patienter med type 2-diabetes, der tidligere blev behandlet med oral middelterapi (undersøgelser E og F)
| Undersøgelse E | Undersøgelse F | |||||||
|---|---|---|---|---|---|---|---|---|
| Exubera + SU* | Mødte*+ SU* | Exubera + SU* | Mødte*+ SU* | Exubera + Met* | Gli* + Met* | Exubera + Met* | Gli* + Met* | |
| Højt stratum†| Lavt lag†| Højt stratum†| Lavt lag†| |||||
| Prøvestørrelse | 113 | 103 | 101 | 93 | 109 | 103 | 125 | 119 |
| ||||||||
| HbA1c (%) | ||||||||
| Baseline middelværdi | 10.5 | 10.6 | 8.8 | 8.8 | 10.4 | 10.6 | 8.6 | 8.7 |
| Adj. gennemsnitlig ændring fra baseline | -2.2 | -1.8 | -1.9 | -1.9 | -2.2 | -1.9 | -1.8 | -1.9 |
| Exubera minus OAc | -0.38c, § | -0.07 | -0.37c, ¶ | 0.04 | ||||
| 95% CI for behandlingsforskel | (-0.63, -0.14) | (-0.33, 0.19) | (-0.62, -0.12) | (-0.19, 0.27) | ||||
| Fastende plasma-glukose (mg / dL) | ||||||||
| Baseline middelværdi | 241 | 237 | 197 | 198 | 223 | 243 | 187 | 196 |
| Gennemsnitlig ændring fra baseline | -46 | -47 | -48 | -52 | -42 | -40 | -46 | -49 |
| Exubera minus OA | 1 | 4 | -2 | 4 | ||||
| 95% CI for behandlingsforskel | (-11, 12) | (-8, 16) | (-14, 10) | (-7, 15) | ||||
| Emner med slutningen af studiet HbA1c < 8%# | 48.7% | 44.7% | 81.2% | 73.1% | 72.5% | 56.3% | 80.8% | 86.6% |
| Emner med slutningen af studiet HbA1c < 7% | 20.4% | 14.6% | 30.7% | 32.3% | 33.9% | 17.5% | 40.0% | 42.9% |
| Kropsvægt | ||||||||
| Baseline middelværdi (kg) | 80.8 | 79.5 | 79.9 | 81.9 | 88.3 | 87.8 | 90.3 | 88.2 |
| Adj. gennemsnitlig ændring fra baseline (kg) | 3.6 | -0.0 | 2.4 | -0.3 | 2.8 | 2.5 | 2.0 | 1.6 |
| Exubera minus OA | 3.60 | 2.67 | 0.26 | 0.38 | ||||
| 95% CI for behandlingsforskel | (2.81, 4.39) | (1.84, 3.51) | (-0.70, 1.21) | (-0.52, 1.27) |
Brug til patienter, der tidligere blev behandlet med subkutan insulin
En 24-ugers, randomiseret, open-label, aktiv-kontrol-undersøgelse (undersøgelse G) blev udført hos insulinbehandlede patienter med type 2 diabetes til vurdering af sikkerheden og effektiviteten af Exubera administreret TID før måltid med en enkelt natinjektion af Humulin® U Ultralente® (n = 146) sammenlignet med subkutant regelmæssigt humant insulin indgivet BID (før morgenmad og før middagen) med BID-injektion af NPH humant insulin (n = 149). I denne undersøgelse var middelalderen 57,5 år (interval: 23-80), 66% af forsøgspersoner var mandlige, og det gennemsnitlige kropsmasseindeks var 30,3 kg / m2.
Reduktionerne fra baseline i HbA1cprocent af patienterne, der når en HbA1c niveau på <8% (pr. behandling af American Diabetes Association-handlingsniveau på tidspunktet for undersøgelsens gennemførelse) og en HbA1c niveau på <7% såvel som hyppigheden af hypoglykæmi var ens mellem behandlingsgrupper. Exubera-behandlede patienter havde en større reduktion i fastende plasmaglukose end patienter i sammenligningsgruppen. Resultaterne for undersøgelse G er vist i tabel 5.
Tabel 5: Resultater af en 24-ugers aktiv-kontrol, open-label-undersøgelse hos patienter med type 2-diabetes, der tidligere blev behandlet med subkutan insulin (undersøgelse G)
| Undersøgelse G | Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) |
|---|---|---|
| Prøvestørrelse | 146 | 149 |
| UL = Humulin® U Ultralente®; SC R = subkutant almindeligt humant insulin | ||
| ||
| HbA1c (%) | ||
| Baseline middelværdi | 8.1 | 8.2 |
| Adj. gennemsnitlig ændring fra baseline | -0.7 | -0.6 |
| Exubera minus SC R* | -0.07 | |
| 95% CI for behandlingsforskel | (-0.31, 0.17) | |
| Fastende plasma-glukose (mg / dL) | ||
| Baseline middelværdi | 152 | 159 |
| Adj. gennemsnitlig ændring fra baseline | -22 | -6 |
| Exubera minus SC R | -16.36 | |
| 95% CI for behandlingsforskel | (-27.09, -5.36) | |
| Patienter med slutningen af undersøgelsen HbA1c < 8%†| 76.0% | 69.1% |
| Patienter med slutningen af undersøgelsen HbA1c < 7% | 45.2% | 32.2% |
| Kropsvægt | ||
| Baseline middelværdi (kg) | 90.6 | 89.0 |
| Adj. gennemsnitlig ændring fra baseline (kg) | 0.1 | 1.3 |
| Exubera minus SC R | -1.28 | |
| 95% CI for behandlingsforskel | (-1.96, -0.60) | |
| Slut på studiens daglige insulindosis | ||
| Kortvirkende insulin | 16,6 mgc | 25,5 IE |
| Langtidsvirkende insulin | 37,9 IE | 52,3 IE |
top
Indikationer og anvendelse
Exubera er indiceret til behandling af voksne patienter med diabetes mellitus til kontrol af hyperglykæmi. Exubera har et begyndende virkning svarende til hurtigvirkende insulinanaloger og har en varighed af glukosesænkende aktivitet sammenlignet med subkutant indgivet almindeligt humant insulin. Hos patienter med type 1-diabetes skal Exubera bruges i regimer, der indeholder et længerevirkende insulin. Hos patienter med type 2-diabetes kan Exubera bruges som monoterapi eller i kombination med orale midler eller længerevirkende insuliner.
top
Kontraindikationer
Exubera er kontraindiceret hos patienter, der er overfølsomme over for Exubera eller et af dets hjælpestoffer.
Exubera er kontraindiceret til patienter, der ryger, eller som har ophørt med at ryge mindre end 6 måneder, før Exubera-behandlingen påbegyndes. Hvis en patient begynder eller fortsætter med at ryge, skal Exubera seponeres straks på grund af den øgede risiko for hypoglykæmi, og en alternativ behandling skal anvendes (se KLINISK FARMAKOLOGI, Særlige befolkninger, Rygning). Sikkerheden og effekten af Exubera hos patienter, der ryger, er ikke fastlagt.
Exubera er kontraindiceret til patienter med ustabil eller dårligt kontrolleret lungesygdom på grund af store variationer ved lungefunktion, der kan påvirke absorptionen af Exubera og øge risikoen for hypoglykæmi eller hyperglykæmi.
top
Advarsler
Exubera adskiller sig fra almindeligt humant insulin ved dets hurtige virkning. Når det bruges som måltidsinsulin, skal dosen af Exubera gives inden for 10 minutter før et måltid.
Hypoglykæmi er den mest hyppigt rapporterede bivirkning ved insulinbehandling, herunder Exubera. Tidspunktet for hypoglykæmi kan variere mellem forskellige insulinformuleringer.
Patienter med diabetes type 1 har også brug for et længerevirkende insulin for at opretholde passende glukosekontrol.
Enhver ændring af insulin skal foretages med forsigtighed og kun under medicinsk kontrol. Ændringer i insulinstyrke, fabrikant, type (f.eks. Regelmæssig, NPH, analoger) eller arter (dyr, menneske) kan resultere i behovet for en ændring i dosis. Samtidig oral antidiabetisk behandling kan muligvis tilpasses.
Glukoseovervågning anbefales til alle patienter med diabetes.
På grund af virkningen af Exubera på lungefunktionen, bør alle patienter have en lungefunktion vurderet, inden behandlingen med Exubera påbegyndes (se FORHOLDSREGLER: Lungefunktion).
Brug af Exubera til patienter med underliggende lungesygdom, såsom astma eller KOL, anbefales ikke, fordi sikkerheden og effekten af Exubera i denne population ikke er blevet fastlagt (se FORHOLDSREGLER: Underliggende lungesygdom).
I kliniske forsøg med Exubera har der været 6 nydiagnosticerede tilfælde af primær lunge malignitet blandt Exubera-behandlede patienter, og 1 nyligt diagnosticeret tilfælde blandt komparatorbehandlede patienter. Der er også blevet rapporteret en postmarkedsføring af en primær lungemalignitet hos en Exubera-behandlet patient. I kontrollerede kliniske forsøg med Exubera var forekomsten af ny primær lungekræft pr. 100 patientår af eksponering af lægemidlet 0,13 (5 tilfælde over 3900 patientår) for Exubera-behandlede patienter og 0,02 (1 tilfælde over 4100 patientår) for komparatorbehandlede patienter. Der var for få tilfælde til at bestemme, om fremkomsten af disse begivenheder er relateret til Exubera. Alle patienter, der blev diagnosticeret med lungekræft, havde en tidligere historie med cigaretrygning.
top
Forholdsregler
Generel
Som med alle insulinpræparater kan tidsforløbet for Exubera-handling variere i forskellige individer eller på forskellige tidspunkter hos det samme individ. Justering af dosis af insulin kan være nødvendigt, hvis patienter ændrer deres fysiske aktivitet eller deres sædvanlige måltider. Insulinbehov kan ændres under sammenhængende tilstande, såsom sygdom, følelsesmæssige forstyrrelser eller stress.
hypoglykæmi
Som med alle insulinpræparater kan hypoglykæmiske reaktioner være forbundet med administrationen af Exubera. Hurtige ændringer i serumglukosekoncentrationer kan inducere symptomer, der ligner hypoglykæmi hos personer med diabetes, uanset glukoseværdien. Tidlige advarselssymptomer på hypoglykæmi kan være forskellige eller mindre udtalt under visse betingelser, såsom lang varighed af diabetes, diabetisk nervesygdom, brug af medicin såsom beta-blokkere eller intensiveret diabeteskontrol (se FORHOLDSREGLER: Stofinteraktion). Sådanne situationer kan resultere i svær hypoglykæmi (og muligvis tab af bevidsthed) inden patienters bevidsthed om hypoglykæmi.
Nedsat nyrefunktion
Der er ikke udført undersøgelser hos patienter med nedsat nyrefunktion. Som med andre insulinpræparater kan dosisbehovene til Exubera reduceres hos patienter med nedsat nyrefunktion (se KLINISK FARMAKOLOGI, Særlige befolkninger).
Nedsat leverfunktion
Der er ikke udført undersøgelser hos patienter med nedsat leverfunktion. Som med andre insulinpræparater kan dosisbehovene til Exubera reduceres hos patienter med nedsat leverfunktion (se KLINISK FARMAKOLOGI, Særlige befolkninger).
Allergi
Systemisk allergi
I kliniske studier var den samlede forekomst af allergiske reaktioner hos patienter, der blev behandlet med Exubera, den samme som hos patienter, der bruger subkutane regimer med almindeligt humant insulin.
Som med andre insulinpræparater kan der forekomme sjældne, men potentielt alvorlige, generelle allergier over for insulin, hvilket kan forårsage udslæt (inklusive kløe) over hele kroppen, åndenød, vejrtrækning, reduktion i blodtryk, hurtig puls eller sveden. Alvorlige tilfælde af generaliseret allergi, inklusive anafylaktiske reaktioner, kan være livstruende. Hvis sådanne reaktioner opstår fra Exubera, skal Exubera stoppes og alternative behandlinger overvejes.
Antistofproduktion
Insulinantistoffer kan udvikles under behandling med alle insulinpræparater inklusive Exubera. I kliniske studier af Exubera, hvor komparatoren var subkutan insulin, steg stigninger i insulinantistofniveauer (som reflekteret ved assays insulinbindingsaktivitet) var signifikant større for patienter, der modtog Exubera end for patienter, der modtog subkutan insulin kun. Ingen kliniske konsekvenser af disse antistoffer blev identificeret i tidsperioden for kliniske studier af Exubera; den langsigtede kliniske betydning af denne stigning i dannelse af antistof er imidlertid ukendt.
Respiratory
Lungefunktion
I kliniske forsøg op til to års varighed viste patienter, der blev behandlet med Exubera, et større fald i lungefunktion, specifikt det tvungne ekspirationsvolumen på et sekund (FEV1) og kulilte-diffusionsevnen (DLCO) end komparatorbehandlet patienter. Den gennemsnitlige behandlingsgruppeforskel i lungefunktion, der favoriserer komparatorgruppen, blev bemærket inden for de første flere uger af behandlingen med Exubera og ændrede sig ikke i løbet af den to år lange behandlingsperiode (Se BIVIRKNINGER: Lungefunktion).
Under de kontrollerede kliniske forsøg oplevede individuelle patienter markante fald i lungefunktion i begge behandlingsgrupper. Et fald fra baseline FEV1 på â € ¥ 20% ved sidst observation forekom hos 1,5% af Exubera-behandlede og 1,3% af de komparatorbehandlede patienter. Et fald fra basislinjen DLCO af â € 20% ved sidst observation forekom hos 5,1% af Exubera-behandlede og 3,6% af de komparatorbehandlede patienter.
På grund af virkningen af Exubera på lungefunktionen, bør alle patienter vurderes med spirometri (FEV1), inden de påbegynder behandling med Exubera. Vurdering af DLCO bør overvejes. Effekten og sikkerheden af Exubera hos patienter med FEV-baseline1 eller DLCO <70% forudsagt er ikke blevet konstateret, og brugen af Exubera i denne population anbefales ikke.
Vurdering af lungefunktion (f.eks. Spirometri) anbefales efter de første 6 måneder af terapien og derefter årligt, selv i fravær af lungesymptomer. Hos patienter, der har et fald på 20% i FEV1 fra basislinien, skal lungefunktionsundersøgelser gentages. Hvis tilbagegangen på 20% fra grundlinjen FEV1 bekræftes, skal Exubera afbrydes. Tilstedeværelsen af lungesymptomer og mindre fald i lungefunktionen kan kræve hyppigere overvågning af lungefunktion og overvejelse om seponering af Exubera.
Underliggende lungesygdom
Brug af Exubera til patienter med underliggende lungesygdom, såsom astma eller KOL, anbefales ikke, fordi Exuberas effekt og sikkerhed i denne population ikke er fastlagt.
bronkospasmer
Der er sjældent rapporteret om bronkospasme hos patienter, der tager Exubera. Patienter, der oplever en sådan reaktion, skal afbryde Exubera og straks søge medicinsk evaluering. Genadministration af Exubera kræver en omhyggelig risikovurdering og bør kun udføres under nøje medicinsk overvågning med passende tilgængelige kliniske faciliteter.
Intercurrent respiratorisk sygdom
Exubera er blevet administreret til patienter med interkurrent luftvejssygdom (f.eks. Bronkitis, infektioner i øvre luftveje, rhinitis) under kliniske studier. Hos patienter, der oplever disse tilstande, stoppede 3-4% midlertidigt Exubera-behandlingen. Der var ingen øget risiko for hypoglykæmi eller forværret glykæmisk kontrol observeret hos Exubera-behandlede patienter sammenlignet med patienter behandlet med subkutant insulin. Under intercurrent luftvejssygdom kan det være nødvendigt med nøje overvågning af blodsukkerkoncentrationer og dosisjustering.
Oplysninger til patienter
Patienter skal instrueres i selvledelsesprocedurer, herunder glukosemonitorering; korrekt Exubera inhalationsteknik; og håndtering af hypoglykæmi og hyperglykæmi. Patienterne skal instrueres i håndtering af specielle situationer, som f.eks. Strømtilstande (sygdom, stress eller følelsesmæssig) forstyrrelser), en utilstrækkelig eller sprunget insulindosis, utilsigtet indgivelse af en forøget insulindosis, utilstrækkelig madindtag, eller sprunget måltider.
Patienter skal informeres om, at behandling i Exubera i kliniske studier var forbundet med små, ikke-progressive middelfald i lungefunktionen i forhold til komparatorbehandlinger. På grund af virkningen af Exubera på lungefunktion anbefales lungefunktionstest, inden behandlingen med Exubera påbegyndes. Efter påbegyndelse af behandlingen anbefales periodiske lungefunktionstest (se FORHOLDSREGLER Åndedrætsværn, lungefunktion).
Patienter skal informere deres læge, hvis de har haft en lungesygdom, fordi brug af Exubera ikke anbefales i patienter med underliggende lungesygdom (f.eks. astma eller KOL) og er kontraindiceret til patienter med dårligt kontrolleret lunge sygdom.
Kvinder med diabetes bør rådes til at informere deres læge, hvis de er gravide eller overvejer graviditet.
top
Lægemiddelinteraktioner
Et antal stoffer påvirker glukosemetabolismen og kan kræve justering af insulindosis og særlig nøje overvågning.
Følgende er eksempler på stoffer, der kan reducere den blodsukkersænkende effekt af insulin, der kan resultere i hyperglykæmi: kortikosteroider, danazol, diazoxid, diuretika, sympatomimetiske midler (f.eks. epinephrin, albuterol, terbutalin), glucagon, isoniazid, phenothiazinderivater, somatropin, skjoldbruskkirtelhormoner, østrogener, progestogener (f.eks. i orale prævention), proteaseinhibitorer og atypiske antipsykotiske medikamenter (f.eks. olanzapin og clozapin).
Følgende er eksempler på stoffer, der kan øge den blodglukosesænkende effekt af insulin og modtagelighed for hypoglykæmi: oral antidiabetika, ACE-hæmmere, disopyramid, fibrater, fluoxetin, MAO-hæmmere, pentoxifylline, propoxyphen, salicylater og sulfonamid antibiotika.
Betablokkere, klonidin, lithiumsalte og alkohol kan enten øge eller reducere insulinens blodsukkersænkende virkning. Pentamidin kan forårsage hypoglykæmi, som undertiden kan følges af hyperglykæmi.
Under påvirkning af sympatolytiske lægemidler, såsom betablokkere, clonidin, guanethidin og reserpin, kan tegnene og symptomerne på hypoglykæmi reduceres eller være fraværende.
Bronchodilatorer og andre inhalerede produkter kan ændre absorptionen af inhaleret humant insulin (se KLINISK FARMAKOLOGI, Særlige befolkninger). Det anbefales konsistent tidspunkt for dosering af bronchodilatorer i forhold til Exubera-administration, nøje overvågning af blodglukosekoncentrationer og dosis titrering efter behov.
Karcinogenese, mutagenese, forringelse af fertilitet
To-årige carcinogenicitetsundersøgelser hos dyr er ikke blevet udført. Insulin var ikke mutagent i Ames-bakteriel reversmutationstest i nærvær og fravær af metabolisk aktivering.
Hos Sprague-Dawley-rotter blev der udført en 6-måneders toksicitetsundersøgelse med gentagen dosering med insulininhalationspulver i doser op til 5,8 mg / kg / dag (sammenlignet med den kliniske startdosis på 0,15 mg / kg / dag, den høje dosis af rotter var 39 gange eller 8,3 gange den kliniske dosis, baseret på enten en mg / kg eller en mg / m2 kropsoverfladeareal sammenligning). Hos Cynomolgus-aber blev der udført en 6-måneders toksicitetsundersøgelse med gentagen dosering med inhaleret insulin i doser op til 0,64 mg / kg / dag. Sammenlignet med den kliniske startdosis på 0,15 mg / kg / dag var den høje dosis af abe 4,3 gange eller 1,4 gange den kliniske dosis, baseret på enten en mg / kg eller en mg / m2 kropsoverfladeareal. Disse var maksimalt tolererede doser baseret på hypoglykæmi.
Sammenlignet med kontroldyr var der ingen behandlingsrelaterede bivirkninger hos hverken arter på lungefunktion, grov eller mikroskopisk morfologi i luftvejene eller bronchiale lymfeknuder. Tilsvarende var der ingen virkning på celleproliferationsindekser i alveolar eller bronchiolar område af lungen hos nogen af arterne.
Da rekombinant humant insulin er identisk med det endogene hormon, blev reproduktions- / fertilitetsundersøgelser ikke udført på dyr.
Graviditet
Teratogene effekter
Graviditet kategori C
Dyreproduktionsundersøgelser er ikke blevet udført med Exubera. Det vides heller ikke, om Exubera kan forårsage fosterskade, når det administreres til en gravid kvinde, eller om Exubera kan påvirke reproduktionskapaciteten. Exubera bør kun gives til en gravid kvinde, hvis det er klart nødvendigt.
Sygeplejerske mødre
Mange lægemidler, inklusive humaninsulin, udskilles i modermælk. Af denne grund skal der udvises forsigtighed, når Exubera administreres til en ammende kvinde. Patienter med diabetes, som ammer, kan kræve justeringer i Exubera-dosis, måltider eller begge dele.
Pædiatrisk brug
Langvarig sikkerhed og effektivitet af Exubera hos pædiatriske patienter er ikke fastslået (se KLINISK FARMAKOLOGI, Særlige befolkninger).
Geriatrisk brug
I kontrollerede kliniske fase 2/3 studier (n = 1975) blev Exubera administreret til 266 patienter, 65 år og 30 patienter, 75 år gamle. Størstedelen af disse patienter havde type 2-diabetes. Ændringen i HbA1C og frekvensen af hypoglykæmi adskiller sig ikke efter alder.
top
Bivirkninger
Sikkerheden ved Exubera alene eller i kombination med subkutan insulin eller orale midler har været evalueret i ca. 2500 voksne patienter med type 1 eller type 2 diabetes, der blev udsat for Exubera. Cirka 2000 patienter blev udsat for Exubera i mere end 6 måneder og mere end 800 patienter blev udsat for mere end 2 år.
Ikke-respiratoriske bivirkninger
Ikke-respiratoriske bivirkninger rapporteret hos 1% af 1977 Exubera-behandlede patienter i kontrollerede kliniske fase 2/3-studier, uanset årsagssammenhæng, inkluderer (men er ikke begrænset til) følgende:
Metabolsk og ernæringsmæssig: hypoglykæmi (se ADVARSLER og FORHOLDSREGLER)
Krop som helhed: brystsmerter
Fordøjelse: tør mund
Særlige sanser: otitis media (type 1 pædiatriske diabetikere)
hypoglykæmi
Hastighederne og forekomsten af hypoglykæmi var sammenlignelige mellem Exubera og subkutant almindeligt humant insulin hos patienter med type 1 og type 2 diabetes. Hos type 2-patienter, der ikke var tilstrækkeligt kontrolleret med terapi med enkelt oralt middel, tilføjede Exubera var forbundet med en højere rate af hypoglykæmi end tilføjelsen af en anden oral agent.
Brystsmerter
En række forskellige brystsymptomer blev rapporteret som bivirkninger og blev grupperet under det ikke-specifikke udtryk brystsmerter. Disse hændelser forekom hos 4,7% af Exubera-behandlede patienter og 3,2% af patienterne i sammenligningsgrupper. Størstedelen (> 90%) af disse hændelser blev rapporteret som mild eller moderat. To patienter i Exubera og en i komparatorgruppen stoppede behandlingen på grund af smerter i brystet. Forekomsten af bivirkninger i al årsagssammenhæng relateret til koronar arteriesygdom, såsom angina pectoris eller myokardieinfarkt, var sammenlignelig i Exubera (0,7% angina pectoris; 0,7% hjerteinfarkt) og komparator (1,3% angina pectoris; 0,7% hjerteinfarkt) behandlingsgrupper.
Tør mund
Mundtørhed blev rapporteret hos 2,4% af de Exubera-behandlede patienter og 0,8% af patienterne i sammenligningsgrupper. Næsten alle (> 98%) rapporterede mundtørhed var mild eller moderat. Ingen patienter stoppede behandlingen på grund af mundtørhed.
Ørehændelser hos pædiatriske diabetikere
Pædiatriske type 1-diabetikere i Exubera-grupper oplevede hyppigere bivirkninger relateret til øret, end pædiatriske type 1-diabetikere i behandlingsgrupper, der kun modtog subkutant insulin. Disse begivenheder omfattede otitis media (Exubera 6,5%; SC 3,4%), øre smerter (Exubera 3,9%; SC 1,4%) og øreproblemer (Exubera 1,3%; SC 0%).
Respiratoriske bivirkninger
Tabel 6 viser hyppigheden af respiratoriske bivirkninger for hver behandlingsgruppe, der blev rapporteret i â 1 ¥ af enhver behandlingsgruppe i kontrollerede kliniske fase 2 og 3 studier, uanset årsagssammenhæng.
Tabel 6: Respiratoriske bivirkninger rapporteret i ¥ 1% af enhver behandlingsgruppe i kontrolleret fase 2 og 3 kliniske studier, uanset årsagssammenhæng
| Procent af patienter, der rapporterer begivenhed | |||||
|---|---|---|---|---|---|
| Bivirkning | Type 1 Diabetes | Type 2 Diabetes | |||
| Exubera N = 698 |
SC N = 705 |
Exubera N = 1279 |
SC N = 488 |
OAs N = 644 |
|
| SC = subkutan insulin-komparator; OA = orale middelkomparatorer | |||||
| Luftvejsinfektion | 43.3 | 42.0 | 29.2 | 38.1 | 19.7 |
| Hoste øget | 29.5 | 8.8 | 21.9 | 10.2 | 3.7 |
| Pharyngitis | 18.2 | 16.6 | 9.5 | 9.6 | 5.9 |
| Rhinitis | 14.5 | 10.9 | 8.8 | 10.5 | 3.0 |
| Bihulebetændelse | 10.3 | 7.4 | 5.4 | 10.0 | 2.3 |
| Åndedrætsforstyrrelse | 7.4 | 4.1 | 6.1 | 10.2 | 1.7 |
| dyspnø | 4.4 | 0.9 | 3.6 | 2.5 | 1.4 |
| Sputum øget | 3.9 | 1.3 | 2.8 | 1.0 | 0.5 |
| bronkitis | 3.2 | 4.1 | 5.4 | 3.9 | 4.0 |
| Astma | 1.3 | 1.3 | 2.0 | 2.3 | 0.5 |
| næseblod | 1.3 | 0.4 | 1.2 | 0.4 | 0.8 |
| laryngitis | 1.1 | 0.4 | 0.5 | 0.4 | 0.3 |
| Lungebetændelse | 0.9 | 1.1 | 0.9 | 1.6 | 0.6 |
| Stemmeforandring | 0.1 | 0.1 | 1.3 | 0.0 | 0.3 |
Hoste
I 3 kliniske studier rapporterede patienter, der udfyldte et hoste-spørgeskema, at hosten havde en tendens til at forekomme inden i sekunder til minutter efter Exubera inhalation, var overvejende mild i sværhedsgrad og var sjældent produktiv i natur. Forekomsten af denne hoste faldt med fortsat Exubera-brug. I kontrollerede kliniske studier afsluttede 1,2% af patienterne Exubera-behandling på grund af hoste.
dyspnø
Næsten alle (> 97%) af dyspnø blev rapporteret som mild eller moderat. Et lille antal Exubera-behandlede patienter (0,4%) stoppede behandlingen på grund af dyspnø sammenlignet med 0,1% af de komparatorbehandlede patienter.
Andre respiratoriske bivirkninger - Faryngitis, øget sputum og epistaxis
Størstedelen af disse begivenheder blev rapporteret som milde eller moderate. Et lille antal Exubera-behandlede patienter stoppede behandlingen på grund af faryngitis (0,2%), og sputum steg (0,1%); ingen patienter stoppede behandlingen på grund af epistaxis.
Lungefunktion
Virkningen af Exubera på åndedrætsorganerne er blevet evalueret hos over 3800 patienter i kontrollerede kliniske fase 2- og 3-studier (hvor 1977 patienter blev behandlet med Exubera). I randomiserede, åbne kliniske forsøg op til to års varighed blev patienter behandlet med Exubera påviste et større fald i lungefunktion, specifikt det tvungne ekspirationsvolumen i et sekund (FEV1) og carbonmonoxid-diffusionsevne (DLCO) end patienter, der behandlede komparatorer. De gennemsnitlige behandlingsgruppeforskelle i FEV1 og DLCO, blev noteret inden for de første flere uger af behandlingen med Exubera og forløb ikke i løbet af den to år lange behandlingsperiode. I et afsluttet kontrolleret klinisk forsøg hos patienter med type 2-diabetes efter to års behandling med Exubera, viste patienter opløsning af behandlingsgruppeforskellen i FEV1 seks uger efter seponering af behandlingen. Opløsning af virkningen af Exubera på lungefunktion hos patienter med type 1-diabetes er ikke undersøgt efter langtidsbehandling.
Figur 3 til 6 viser den gennemsnitlige FEV1 og DLCO ændring fra baseline versus tid fra to igangværende randomiserede, open-label, to-årige studier på 580 patienter med type 1 og 620 patienter med type 2-diabetes.
Figur 3: Skift fra baseline FEV1 (L) hos patienter med type 1-diabetes (middelværdi +/- standardafvigelse)

Figur 4: Skift fra baseline FEV1 (L) hos patienter med type 2-diabetes (gennemsnit +/- standardafvigelse)

Efter 2 års Exubera-behandling hos patienter med type 1 og type 2-diabetes er forskellen mellem behandlingsgrupper for den gennemsnitlige ændring fra basislinjen FEV1 var ca. 40 ml, hvilket favoriserede komparator.
Figur 5: Skift fra basislinje DLco (ml / min / mmHg) hos patienter med type 1-diabetes (gennemsnit +/- standardafvigelse)
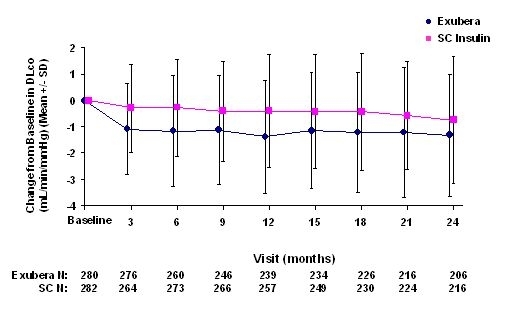
Figur 6: Skift fra basislinje DLco (ml / min / mmHg) hos patienter med type 2-diabetes (gennemsnit +/- standardafvigelse)

Efter 2 års Exubera-behandling var forskellen mellem behandlingsgrupper for den gennemsnitlige ændring fra basislinien DLCO 0,5 ml / min / mmHg (type 1-diabetes), hvor foretrukket komparator var, og ca. 0,1 ml / min / mmHg (type 2-diabetes), hvilket favoriserede Exubera.
I de to-årige kliniske forsøg oplevede individuelle patienter markante fald i lungefunktion i begge behandlingsgrupper. Et fald fra grundlinjen FEV1 af â € 20% ved sidst observation forekom hos 1,5% af Exubera-behandlede og 1,3% af de komparatorbehandlede patienter. Et fald fra basislinjen DLCO af â € 20% ved sidst observation forekom hos 5,1% af Exubera-behandlede og 3,6% af de komparatorbehandlede patienter.
top
overdosering
Hypoglykæmi kan forekomme som et resultat af et overskud af insulin i forhold til fødeindtagelse, energiudgifter eller begge dele.
Mild til moderat afsnit af hypoglykæmi kan normalt behandles med oral glukose. Justeringer i lægemiddeldosering, måltidsmønstre eller træning kan være nødvendige.
Alvorlige episoder med hypoglykæmi med koma, anfald eller neurologisk svækkelse kan behandles med intramuskulær / subkutan glukagon eller koncentreret intravenøs glukose. Vedvarende indtagelse af kulhydrater og observation kan være nødvendigt, fordi hypoglykæmi kan gentage sig efter tilsyneladende klinisk bedring.
top
Dosering og administration
Exubera har ligesom hurtigvirkende insulinanaloger en hurtigere begyndelse af glukosesænkende aktivitet sammenlignet med subkutant injiceret almindeligt humant insulin. Exubera har en varighed af glukosesænkende aktivitet sammenlignelig med subkutant injektion af almindeligt humant insulin og længere end hurtigvirkende insulin. Exubera-doser skal administreres umiddelbart før måltiderne (højst 10 minutter før hvert måltid).
Hos patienter med type 1-diabetes skal Exubera bruges i regimer, der indeholder et længerevirkende insulin. For patienter med type 2-diabetes kan Exubera anvendes som monoterapi eller i kombination med orale midler eller længerevirkende insulin.
På grund af virkningen af Exubera på lungefunktion, skal alle patienter have en lungefunktion vurderet, inden behandlingen med Exubera påbegyndes. Periodisk overvågning af lungefunktion anbefales til patienter, der behandles med Exubera (se FORHOLDSREGLER, Lungefunktion).
Exubera er beregnet til indgivelse ved indånding og må kun administreres ved hjælp af Exubera® Inhaler. Henvis til Guide til Exubera-medicin til en beskrivelse af Exubera® Inhalator og instruktioner til brug af inhalatoren.
Beregning af den oprindelige exubera-dosis før måltid
Den indledende dosis af Exubera skal individualiseres og bestemmes på baggrund af lægeens råd i overensstemmelse med patientens behov. Anbefalede første doser før måltidet er baseret på kliniske forsøg, hvor patienterne blev anmodet om at spise tre måltider pr. Dag. De indledende doser før måltidet kan beregnes ved hjælp af følgende formel: [Kropsvægt (kg) X 0,05 mg / kg = dosis før måltid (mg)] afrundet til det nærmeste hele milligramtal (f.eks. 3,7 mg afrundet til 3 mg).
Omtrentlige retningslinjer for indledende Exubera-doser før måltid, baseret på patientens kropsvægt, er angivet i tabel 7:
Tabel 7: Tilnærmede retningslinjer for initial exuberadosis før måltid (baseret på patientens kropsvægt)
| Patientvægt (i kg) |
Patientvægt (i lb) |
Startdosis pr. Måltid | Antal 1 mg blister per dosis | Antal 3 mg blister per dosis |
|---|---|---|---|---|
| 30 til 39,9 kg | 66 - 87 lb | 1 mg pr. Måltid | 1 | - |
| 40 til 59,9 kg | 88 - 132 lb | 2 mg pr. Måltid | 2 | - |
| 60 til 79,9 kg | 133 - 176 pund | 3 mg pr. Måltid | - | 1 |
| 80 til 99,9 kg | 177 - 220 lb | 4 mg pr. Måltid | 1 | 1 |
| 100 til 119,9 kg | 221- 264 pund | 5 mg pr. Måltid | 2 | 1 |
| 120 til 139,9 kg | 265 - 308 pund | 6 mg pr. Måltid | - | 2 |
En 1 mg blisterflaske med Exubera inhaleret insulin svarer omtrent til 3 IE subkutant injektion af almindeligt humant insulin. En 3 mg blisterflaske med Exubera inhaleret insulin svarer til ca. 8 IE subkutant injiceret almindeligt humant insulin. Tabel 8 viser den omtrentlige IE-dosis af regelmæssigt subkutant humant insulin til Exubera inhalerede insulindoser fra 1 mg til 6 mg.
Tabel 8: Omtrentlig ækvivalent IE-dosis af regelmæssigt humant subkutant insulin til exubera inhalerede insulindoser i området fra 1 mg til 6 mg
| Dosis (mg) | Omtrentlig regelmæssig SC-dosis til insulin i IU | Antal 1 mg Exubera-blister pr. Dosering | Antal 3 mg Exubera-blister pr. Dosering |
|---|---|---|---|
| 1 mg | 3 | 1 | - |
| 2 mg | 6 | 2 | - |
| 3 mg | 8 | - | 1 |
| 4 mg | 11 | 1 | 1 |
| 5 mg | 14 | 2 | 1 |
| 6 mg | 16 | - | 2 |
Patienter skal kombinere 1 mg og 3 mg blister, så der tages mindst mulig antal blister pr. Dosis (f.eks. Bør en 4 mg dosis administreres som en 1 mg blister og en 3 mg blister). På hinanden følgende inhalering af tre 1 mg enhedsdosisblister resulterer i signifikant større insulineksponering end inhalation af en 3 mg enhedsdosisblister. Derfor bør tre 1 mg doser ikke erstattes med en 3 mg dosis (se KLINISK FARMAKOLOGIFarmakokinetik). Når en patient er stabiliseret på et doseringsregime, der inkluderer 3 mg blister, og 3 mg blister bliver midlertidigt utilgængelig, kan patienten midlertidigt erstatte to 1 mg blemmer med en 3 mg blister. Blodglukose skal overvåges nøje.
Som med alle insuliner inkluderer yderligere faktorer, der skal tages i betragtning, når Exubera startdosis bestemmes, men er ikke begrænset til, patientens nuværende glykæmiske kontrol, tidligere respons på insulin, varighed af diabetes og diæt og træning vaner.
Overvejelser til dosetitrering
Efter påbegyndt Exubera-behandling, som med andre glukosesænkende midler, kan dosisjustering være nødvendig på grundlag af patientens behov (f.eks. blodglukosekoncentrationer, måltidsstørrelse og næringssammensætning, tid på dagen og nyere eller forventede dyrke motion). Hver patient skal titreres til deres optimale dosis baseret på blodsukkerovervågningsresultater.
Som for alle insuliner kan tidsforløbet for Exubera-handling variere i forskellige individer eller på forskellige tidspunkter hos det samme individ.
Exubera kan anvendes under intercurrent luftvejssygdom (f.eks. Bronkitis, infektion i øvre luftvej, rhinitis). Nøjagtig overvågning af blodsukkerkoncentrationer og dosisjustering kan være påkrævet på individuelt grundlag. Inhalerede lægemidler (f.eks. Bronchodilatorer) bør administreres inden administration af Exubera.
top
Hvordan leveres
Exubera (humant insulin [rDNA-oprindelse]) Inhalationspulver fås i 1 mg og 3 mg enhedsdosisblister. Blisterne udleveres på perforerede kort med seks enhedsdosisblister (PVC / aluminium). De to styrker er differentieret ved farveprint og taktile mærker, der kan differentieres ved berøring. Blister på 1 mg og respektive perforerede kort er trykt med grønt blæk, og kortene er markeret med en hævet bjælke. 3 mg blister og respektive perforerede kort er trykt med blåt blæk, og kortene er markeret med tre hævede bjælker.
Fem blisterkort er pakket i en klar plastformet (PET) termoformet bakke. Hver PET-bakke indeholder også et tørremiddel og er dækket med et klart plastik (PET) låg. Bakken med fem blisterkort (30 enhedsdosisblister) forsegles i en folie-laminatpose med et tørremiddel.
Exubera (humant insulin [rDNA-oprindelse]) Indånding Pulverblister, en Exubera® Inhalator og udskiftning Exubera® Frigørelsesenheder er påkrævet for at starte behandling med Exubera og leveres i Exubera Kit. En fuldstændig samlet Exubera® Inhalator består af inhalatorbasen, et kammer og en Exubera® Slip enhed. En fuldstændig samlet inhalator er pakket med et erstatningskammer og fås i Exubera Kit og som en separat enhed. Afdelingen er også tilgængelig som en individuel komponent.
Exubera® Frigørelsesenheder pakkes individuelt i en forseglet termoformet bakke. Én Exubera® Frigørelsesenhed er inkluderet i hver fuldt monteret inhalator. To ekstra frigørelsesenheder findes i Exubera Kit og i hver kombinationspakke. Exubera frigørelsesenheder er også tilgængelige individuelt.
Se tabel 9 og 10 for en beskrivelse af disse konfigurationer.
Tabel 9
| Exubera (humant insulin [rDNA-oprindelse]) Inhalationspulver fås som følger: | ||
|---|---|---|
| Beskrivelse | Indhold | NDC |
| Exubera KIT | 1 Exubera-inhalator 1 Udskiftningskammer 1 mg - 180 blemmer 3 mg - 90 blemmer 2 Exubera® Slip enheder |
0069-0050-85 |
| Exubera Combination Pack 12 | 1 mg à 90 blemmer 3 mg - 90 blemmer 2 Exubera® Slip enheder |
0069-0050-19 |
| Exubera Combination Pack 15 | 1 mg - 180 blemmer 3 mg - 90 blemmer 2 Exubera® Slip enheder |
0069-0050-53 |
| Exubera 1 mg patientpakke | 90 × 1 mg 2 Exubera® Slip enheder |
0069-0707-37 |
| Exubera 3 mg patientpakke | 90 × 3 mg 2 Exubera® Slip enheder |
0069-0724-37 |
Tabel 10
| Exubera® Inhalator og komponenter fås som følger: | ||
|---|---|---|
| Beskrivelse | Indhold | NDC |
| Exubera® Inhalator og kammer | 1 Exubera® inhaler 1 Udskiftningskammer |
0069-0054-19 |
| Exubera® Slip enheder | 2 Exubera® Slip enheder | 0069-0097-41 |
| Exubera® Kammer | 1 Udskiftningskammer | 0069-0061-19 |
Blisteropbevaring
Ikke i brug (Uåbnet): Opbevares ved kontrolleret stuetemperatur, 25 ° C (77 ° F); udflugter tilladt til 15-30 ° C (59-86 ° F) [se USP kontrolleret rumtemperatur]. Frys ikke. Må ikke køles i køleskab.
I brug: Når folieovertrækningen er åbnet, skal enhedsdosisblister beskyttes mod fugt og opbevares ved 25 ° C (77 ° F); udflugter tilladt til 15-30 ° C (59-86 ° F) [se USP kontrolleret rumtemperatur]. Frys ikke. Må ikke køles i køleskab. Enhedsdosisblister skal bruges inden for 3 måneder efter åbning af folieovertræk. Vend blisterne tilbage til overtrækket for at beskytte mod fugt. Der skal udvises ekstra omhu for at undgå fugtige miljøer, f.eks. dampende badeværelse efter et brusebad.
Kasser blister, hvis de er frosne.
Opbevaring af inhalator
Opbevares ved kontrolleret stuetemperatur, 25 ° C (77 ° F); udflugter tilladt til 15-30 ° C (59-86 ° F) [se USP kontrolleret rumtemperatur]. Frys ikke. Må ikke køles i køleskab.
Exubera® Inhalator kan bruges i op til 1 år fra datoen for første brug.
Udskiftning af Exubera® Slip enhed
Exubera® Slip enhed i Exubera® Inhalator skal udskiftes hver 2. uge.
Holde utilgængeligt for børn
Kun Rx

LAB-0331-12,0
sidste revision 04/2008
Exubera, humant insulin [rDNA-oprindelse] Patientinformation (på almindeligt engelsk)
Detaljeret information om tegn, symptomer, årsager, behandling af diabetes
Oplysningerne i denne monografi er ikke beregnet til at dække alle mulige anvendelser, retninger, forholdsregler, medikamentinteraktion eller ugunstige virkninger. Denne information er generaliseret og er ikke beregnet til specifik medicinsk rådgivning. Hvis du har spørgsmål om de medicin, du tager eller ønsker mere information, skal du kontakte din læge, apotek eller sygeplejerske.
tilbage til: Gennemse alle medicin mod diabetes



