Prandin til behandling af diabetes
Brand name: Prandin
Generisk navn: repaglinide
Indhold:
Beskrivelse
Farmakologi
Indikationer og anvendelse
Kontraindikationer
Forholdsregler
Bivirkninger
Overdosis
Dosis
leveres
Prandin, patientinformation (på almindeligt engelsk)
Beskrivelse
Prandin® (repaglinid) er et oralt blodsukkersænkende medikament i meglitinidklassen, der bruges i behandling af type 2 diabetes mellitus (også kendt som ikke-insulinafhængig diabetes mellitus eller NIDDM). Repaglinid, S (+) 2-ethoxy-4 (2 ((3-methyl-1- (2- (1-piperidinyl) phenyl) -butyl) amino) -2-oxoethyl) benzoesyre, er kemisk ikke relateret til den orale sulfonylurinstofinsulinsekretagoger.
Strukturformlen er som vist nedenfor:
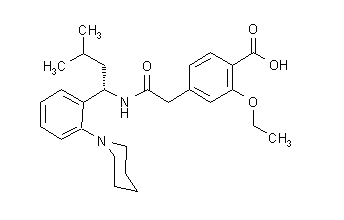
Repaglinid er et hvidt til off-white pulver med molekylformel C27 H36N204 og en molekylvægt på 452,6. Prandin-tabletter indeholder 0,5 mg, 1 mg eller 2 mg repaglinid. Derudover indeholder hver tablet følgende inaktive ingredienser: calciumhydrogenphosphat (vandfrit), mikrokrystallinsk cellulose, majsstivelse, polacrilin-kalium, povidon, glycerol (85%), magnesiumstearat, meglumin, og poloxamer. Tabletterne på 1 mg og 2 mg indeholder jernoxider (henholdsvis gul og rød) som farvestoffer.
top
Klinisk farmakologi
Handlingsmekanisme
Repaglinid sænker blodsukkerniveauet ved at stimulere frigivelsen af insulin fra bugspytkirtlen. Denne handling er afhængig af fungerende beta-celler i bugspytkirtlen. Insulinfrigivelse er glukoseafhængig og formindskes ved lave glukosekoncentrationer.
Repaglinid lukker ATP-afhængige kaliumkanaler i cell-cellemembranen ved binding på karakteriserbare steder. Denne kaliumkanalblokade depolariserer Ÿ-cellen, som fører til en åbning af calciumkanaler. Den resulterende forøgede calciumtilstrømning inducerer insulinudskillelse. Ionkanalmekanismen er meget vævsselektiv med lav affinitet for hjerte- og knoglemuskler.
Farmakokinetik
absorption:
Efter oral administration absorberes repaglinid hurtigt og fuldstændigt fra mave-tarmkanalen. Efter enkle og multiple orale doser hos raske individer eller hos patienter forekommer de maksimale plasmamedicinske niveauer (Cmax) inden for 1 time (Tmax). Repaglinid elimineres hurtigt fra blodstrømmen med en halveringstid på cirka 1 time. Den gennemsnitlige absolutte biotilgængelighed er 56%. Når repaglinid blev givet sammen med mad, blev den gennemsnitlige Tmax ikke ændret, men den gennemsnitlige Cmax og AUC (område under tid / plasmakoncentrationskurven) blev reduceret med henholdsvis 20% og 12,4%.
Fordeling:
Efter intravenøs (IV) dosering hos raske individer var fordelingsvolumenet ved stabil tilstand (Vss) 31 L, og den totale kropsafklaring (CL) var 38 L / h. Proteinbinding og binding til humant serumalbumin var større end 98%.
Metabolisme:
Repaglinid metaboliseres fuldstændigt ved oxidativ biotransformation og direkte konjugering med glucuronsyre efter enten en IV eller oral dosis. De vigtigste metabolitter er en oxideret dicarboxylsyre (M2), den aromatiske amin (M1) og acylglucuronid (M7). Cytochrome P-450-enzymsystemet, specifikt 2C8 og 3A4, har vist sig at være involveret i N-dealkyleringen af repaglinid til M2 og den yderligere oxidation til M1. Metabolitter bidrager ikke til den glukosesænkende effekt af repaglinid.
udskillelse:
Inden for 96 timer efter dosering med 14C-repaglinid som en enkelt oral oral dosis blev ca. 90% af radiomærket udvundet i fæces og ca. 8% i urinen. Kun 0,1% af dosis ryddes i urinen som moderforbindelse. Den største metabolit (M2) tegnede sig for 60% af den indgivne dosis. Mindre end 2% af lægemidlet blev udvundet i fæces.
Farmakokinetiske parametre:
De farmakokinetiske parametre for repaglinid opnået fra en enkeltdosis, crossover-undersøgelse hos raske individer og fra a multiple-dosis, parallel, dosis-proportionalitet (0,5, 1, 2 og 4 mg) undersøgelse hos patienter med type 2-diabetes er sammenfattet i følgende tabel:
| Parameter | Patienter med type 2-diabetes * |
|
Dosis 0,5 mg 1 mg 2 mg 4 mg |
AUC0-24 timer Gennemsnit ± SD (ng / ml * time): 68.9 ± 154.4 125.8 ± 129.8 152.4 ± 89.6 447.4 ± 211.3 |
|
Dosis 0,5 mg 1 mg 2 mg 4 mg |
Cmax0-5 timer Gennemsnit ± SD (ng / ml): 9.8 ± 10.2 18.3 ± 9.1 26.0 ± 13.0 65.8 ± 30.1 |
|
Dosis 0,5 - 4 mg |
Tmax0-5 timer Midler (SD) 1,0 - 1,4 (0,3 - 0,5) time |
|
Dosis 0,5 - 4 mg |
T ½ Midler (Ind Range) 1,0 - 1,4 (0,4 - 8,0) time |
| Parameter | Sunde emner |
| CL baseret på i.v. | 38 ± 16 l / time |
| Vss baseret på i.v. | 31 ± 12 l |
| AbsBio | 56 ± 9% |
|
CL = total kropsafstand Vss= distributionsvolumen ved stabil tilstand AbsBio = absolut biotilgængelighed |
* doseres forhåndsvis med tre måltider
Disse data indikerer, at repaglinid ikke akkumulerede i serum. Clearance af oralt repaglinid ændrede sig ikke inden for dosisområdet 0,5 - 4 mg, hvilket indikerede et lineært forhold mellem dosis og plasmalægemiddelniveauer.
Eksponeringsvariation:
Repaglinid AUC efter flere doser på 0,25 til 4 mg med hvert måltid varierer over et bredt interval. De intra-individuelle og inter-individuelle variationskoefficienter var henholdsvis 36% og 69%. AUC i det terapeutiske dosisområde omfattede 69 til 1005 ng / ml * time, men AUC-eksponering op til 5417 ng / ml * time blev nået i dosis-eskaleringsundersøgelser uden åbenbare bivirkninger.
Særlige befolkninger:
Geriatrisk:
Sunde frivillige blev behandlet med et regime på 2 mg taget før hver af 3 måltider. Der var ingen signifikante forskelle i farmakokinetikken for repaglinid mellem gruppen af patienter. FORHOLDSREGLER, Geriatrisk anvendelse)
Pædiatrisk:
Der er ikke udført undersøgelser hos pædiatriske patienter.
Køn:
En sammenligning af farmakokinetik hos mænd og kvinder viste AUC i dosisområdet 0,5 mg til 4 mg at være 15% til 70% højere hos kvinder med type 2-diabetes. Denne forskel blev ikke reflekteret i hyppigheden af hypoglykæmiske episoder (han: 16%; kvinde: 17%) eller andre bivirkninger. Med hensyn til køn er der ikke indikeret nogen ændring i den generelle dosisanbefaling, da doseringen for hver patient skal individualiseres for at opnå optimal klinisk respons.
Race:
Der er ikke udført farmakokinetiske undersøgelser for at vurdere virkningen af race, men i et amerikansk 1-årigt studie på patienter med type 2-diabetes, var den blodsukkersænkende effekt sammenlignelig mellem kaukasiere (n = 297) og afroamerikanere (n = 33). I et amerikansk dosis-respons-studie var der ingen tydelig forskel i eksponering (AUC) mellem kaukasiere (n = 74) og Hispanics (n = 33).
Lægemiddelinteraktioner
Lægemiddelinteraktionsundersøgelser udført hos raske frivillige viser, at Prandin ikke havde nogen klinisk relevant effekt på de farmakokinetiske egenskaber af digoxin, theophylline eller warfarin. Samtidig administration af cimetidin med Prandin ændrede ikke signifikant absorption og bortskaffelse af repaglinid.
Derudover blev de følgende lægemidler undersøgt hos raske frivillige med samtidig administration af Prandin. Nedenfor vises resultaterne:
Gemfibrozil og Itraconazole:
Samtidig administration af gemfibrozil (600 mg) og en enkelt dosis på 0,25 mg Prandin (efter 3 dage med to gange dagligt 600 mg gemfibrozil) resulterede i en 8,1 gange højere repaglinid AUC og forlænget repaglinidhalveringstid fra 1,3 til 3,7 timer. Samtidig administration med itraconazol og en enkelt dosis på 0,25 mg Prandin (på den tredje dag af a behandling med 200 mg startdosis, 100 mg itraconazol to gange dagligt) resulterede i en 1,4 gange højere repaglinid AUC. Samtidig administration af både gemfibrozil og itraconazol med Prandin resulterede i en 19 gange højere AUC for repaglinid og forlænget halveringstid for repaglinid til 6,1 timer. Plasmagepaglinidkoncentration 7 timer steg 28,6 gange med gemfibrozil samtidig administration og 70,4 gange med gemfibrozil-itraconazol-kombinationen (se FORHOLDSREGLER, Stof-lægemiddelinteraktioner).
Ketoconazol:
Samtidig indgivelse af 200 mg ketoconazol og en enkelt dosis på 2 mg Prandin (efter 4 dage af én gang) daglig ketoconazol 200 mg) resulterede i en 15% og 16% stigning i repaglinid AUC og Cmax, henholdsvis. Stigningerne var fra 20,2 ng / ml til 23,5 ng / ml for Cmax og fra 38,9 ng / ml * time til 44,9 ng / ml * time i AUC.
rifampin:
Samtidig administration af 600 mg rifampin og en enkelt dosis på 4 mg Prandin (efter 6 dage med en gang daglig 600 mg rifampin) resulterede i et fald på 32% og 26% i AU for repaglinid og Cmax. Faldene var fra 40,4 ng / ml til 29,7 ng / ml for Cmax og fra 56,8 ng / ml * time til 38,7 ng / ml * time i AUC.
I en anden undersøgelse blev samtidig administration af 600 mg rifampin og en enkelt dosis på 4 mg Prandin (efter 6 dage af én gang) dagligt rifampin 600 mg) resulterede i et 48% og 17% fald i repaglinid-median AUC og median Cmax henholdsvis. Medianfaldet var fra 54 ng / ml * time til 28 ng / ml * time for AUC og fra 35 ng / ml til 29 ng / ml for Cmax. Prandin indgivet af sig selv (efter 7 dage med en gang daglig 600 mg rifampin) resulterede i et 80% og 79% fald i henholdsvis repaglinidmedian AUC og Cmax. Faldene var fra 54 ng / ml * time til 11 ng / ml * time for AUC og fra 35 ng / ml til 7,5 ng / ml for Cmax.
Levonorgestrel & Ethinyl Estradiol:
Samtidig administration af en kombinationstablet på 0,15 mg levonorgestrel og 0,03 mg ethinyløstradiol indgivet en gang dagligt i 21 dage med 2 mg Prandin indgivet tre gange dagligt (dag 1-4) og en enkelt dosis på dag 5 resulterede i 20% stigning i repaglinid, levonorgestrel og ethinyløstradiol Cmax. Stigningen i repaglinid Cmax var fra 40,5 ng / ml til 47,4 ng / ml. Ethinyløstradiol AUC-parametre blev forøget med 20%, mens repaglinid- og levonorgestrel AUC-værdier forblev uændrede.
simvastatin:
Samtidig administration af 20 mg simvastatin og en enkelt dosis på 2 mg Prandin (efter 4 dage med simvastatin en gang dagligt 20) mg og tre gange dagligt Prandin 2 mg) resulterede i en 26% stigning i repaglinid Cmax fra 23,6 ng / ml til 29,7 ng / ml. AUC var uændret.
Nifedipine:
Samtidig indgivelse af 10 mg nifedipin med en enkelt dosis på 2 mg Prandin (efter 4 dage af tre gange dagligt nifedipin 10 mg og tre gange dagligt Prandin 2 mg) resulterede i uændrede AUC- og Cmax-værdier for begge lægemidler.
Clarithromycin:
Samtidig indgivelse af 250 mg klarithromycin og en enkelt dosis på 0,25 mg Prandin (efter 4 dage på to gange daglig Clarithromycin 250 mg) resulterede i en 40% og 67% stigning i repaglinid AUC og Cmax, henholdsvis. Stigningen i AUC var fra 5,3 ng / ml * time til 7,5 ng / ml * time, og stigningen i Cmax var fra 4,4 ng / ml til 7,3 ng / ml.
trimethoprim:
Samtidig indgivelse af 160 mg trimethoprim og en enkelt dosis på 0,25 mg Prandin (efter 2 dage to gange dagligt og en dosis på den tredje dag af trimethoprim 160 mg) resulterede i en 61% og 41% stigning i repaglinid AUC og Cmax, henholdsvis. Stigningen i AUC var fra 5,9 ng / ml * time til 9,6 ng / ml * time, og stigningen i Cmax var fra 4,7 ng / ml til 6,6 ng / ml.
Nedsat nyrefunktion
Enkeltdosis og stabil farmakokinetik af repaglinid blev sammenlignet mellem patienter med type 2-diabetes og normal nyrefunktion (CrCl> 80 ml / min), mild til moderat nedsat nyrefunktion (CrCl = 40 - 80 ml / min) og alvorlig nedsat nyrefunktion (CrCl = 20 - 40 ml / min). Både AUC og Cmax for repaglinid var ens hos patienter med normal og mild til moderat nedsat nyrefunktion (middelværdier 56,7 ng / ml * time vs henholdsvis 57,2 ng / ml * time og 37,5 ng / ml vs 37,7 ng / ml.) Patienter med stærkt nedsat nyrefunktion havde forhøjet gennemsnitlig AUC og Cmax værdier (henholdsvis 98,0 ng / ml * time og 50,7 ng / ml), men denne undersøgelse viste kun en svag korrelation mellem repaglinidniveauer og kreatinin clearance. Første dosisjustering ser ikke ud til at være nødvendig for patienter med mild til moderat nyrefunktion. Patienter med type 2-diabetes, der har alvorlig nedsat nyrefunktion, skal imidlertid starte Prandin-behandling med 0,5 mg-dosis - derefter skal patienterne titreres omhyggeligt. Undersøgelser blev ikke udført på patienter med kreatininclearance under 20 ml / min eller patienter med nyresvigt, der krævede hæmodialyse.
Nedsat leverfunktion
En enkeltdosis, open-label-undersøgelse blev udført hos 12 raske forsøgspersoner og 12 patienter med kronisk leversygdom (CLD) klassificeret efter Child-Pugh-skala og koffein-clearance. Patienter med moderat til svær nedsat leverfunktion havde højere og mere langvarige serumkoncentrationer af både total og ubundet repaglinid end raske forsøgspersoner (AUChealth: 91,6 ng / ml * time; AUCCLD patienter: 368,9 ng / ml * time; Cmax, sund: 46,7 ng / ml; Cmax, CLD-patienter: 105,4 ng / ml). AUC var statistisk korreleret med koffeinklarering. Der blev ikke observeret nogen forskel i glukoseprofiler på tværs af patientgrupper. Patienter med nedsat leverfunktion kan udsættes for højere koncentrationer af repaglinid og dets associerede metabolitter end patienter med normal leverfunktion, der får almindelige doser. Prandin bør derfor anvendes forsigtigt til patienter med nedsat leverfunktion. Længere intervaller mellem dosisjusteringer bør anvendes for at muliggøre en fuldstændig vurdering af responsen.
Kliniske forsøg
Monoterapiforsøg
Et fire ugers, dobbeltblindt, placebokontrolleret dosis-respons-forsøg blev udført hos 138 patienter med type 2-diabetes ved anvendelse af doser i intervallet fra 0,25 til 4 mg taget med hver af tre måltider. Prandin-behandling resulterede i dosisproportionel glukosesænkning over hele dosisområdet. Plasmainsulinniveauer steg efter måltiderne og vendte tilbage til baseline før det næste måltid. Det meste af fastende blodsukkersænkende effekt blev påvist inden for 1-2 uger.
I en dobbeltblind, placebokontrolleret 3-måneders dosis titreringstudie blev Prandin eller placebo doser for hver patient steg ugentligt fra 0,25 mg til 0,5, 1 og 2 mg, til maksimalt 4 mg, indtil en fastende plasmaglukose (FPG) niveau
Prandin vs. Placebo-behandling: Gennemsnitlig FPG, PPG og HbA1c Ændringer fra baseline efter 3 måneders behandling:
| ||||||
| FPG (mg / dL) | PPG (mg / dL) | HbA1c (%) | ||||
| PL | R | PL | R | PL | R | |
| Baseline | 215.3 | 220.2 | 245.2 | 261.7 | 8.1 | 8.5 |
|
Skift fra baseline (ved sidste besøg) |
30.3 | -31.0* | 56.5 | -47.6* |
1.1 | -0.6* |
|
FPG = fastende plasmaglukose PPG = postprandial glukose PL = placebo (N = 33) R = repaglinid (N = 66) |
Et andet dobbeltblindt, placebokontrolleret forsøg blev udført hos 362 patienter behandlet i 24 uger. Effekten af præfektielle doser på 1 og 4 mg blev vist ved sænkning af fastende blodsukker og ved HbA1c ved afslutningen af undersøgelsen. HbA1c for de Prandin-behandlede grupper (1 og 4 mg grupper tilsammen) ved afslutningen af undersøgelsen blev reduceret sammenlignet med placebo-behandlede gruppe i tidligere nave patienter og i patienter, der tidligere blev behandlet med orale hypoglykæmiske midler med 2,1% enheder og 1,7% enheder, henholdsvis. I dette forsøg med fast dosis var patienter, der ikke var i stand til oral hypoglykæmisk behandling, og patienter i relativt god glykæmisk kontrol ved baseline (HbA1c under 8%) viste større blodsukkersænkning inklusive en højere frekvens af hypoglykæmi. Patienter, der tidligere blev behandlet og havde baseline HbA1c - 8% rapporterede hypoglykæmi i samme takt som patienter randomiseret til placebo. Der var ingen gennemsnitlig stigning i kropsvægt, når patienter, der tidligere blev behandlet med orale hypoglykæmiske midler, blev skiftet til Prandin. Den gennemsnitlige vægtøgning hos patienter behandlet med Prandin og ikke tidligere behandlet med sulfonylurinstof lægemidler var 3,3%.
Dosen af Prandin i forhold til måltidsrelateret insulinfrigivelse blev undersøgt i tre forsøg inklusive 58 patienter. Glykæmisk kontrol blev opretholdt i en periode, hvor måltidet og doseringsmønsteret blev varieret (2, 3 eller 4 måltider pr. Dag; før måltider x 2, 3 eller 4) sammenlignet med en periode på 3 regelmæssige måltider og 3 doser pr. dag (før måltider x 3). Det blev også vist, at Prandin kan indgives i starten af et måltid, 15 minutter før eller 30 minutter før måltidet med den samme blodsukkersænkende effekt.
Prandin blev sammenlignet med andre insulinsekretagoger i 1-årigt kontrollerede forsøg for at påvise sammenlignelighed af effektivitet og sikkerhed. Hypoglykæmi blev rapporteret hos 16% af 1228 Prandin-patienter, 20% af 417 glyburidpatienter og 19% af 81 glipizidpatienter. Af Prandin-behandlede patienter med symptomatisk hypoglykæmi udviklede ingen koma eller krævede indlæggelse.
Kombinationsforsøg
Prandin blev undersøgt i kombination med metformin hos 83 patienter, der ikke var tilfredsstillende kontrolleret med træning, diæt og metformin alene. Prandin-dosis blev titreret i 4 til 8 uger, efterfulgt af en 3-måneders vedligeholdelsesperiode. Kombinationsterapi med Prandin og metformin resulterede i signifikant større forbedring i glykæmisk kontrol sammenlignet med monagoterapi med repaglinid eller metformin. HbA1c blev forbedret med 1% enhed, og FPG faldt med yderligere 35 mg / dL. I denne undersøgelse, hvor metformindosen blev holdt konstant, viste kombinationsbehandlingen af Prandin og metformin dosisbesparende virkninger med hensyn til Prandin. Den større effektivitetsrespons i kombinationsgruppen blev opnået ved en lavere daglig dosis af repaglinid end i Prandin-monoterapigruppen (se tabel).
Prandin- og metforminbehandling: gennemsnitlige ændringer fra baseline i glykæmiske parametre og vægt efter 4 til 5 måneders behandling *
| Prandin | kombination | Metformin | |
| N | 28 | 27 | 27 |
|
Median endelig dosering (Mg / dag) |
12 |
6 (Prandin) 1500 (metformin) |
1500 |
| HbA1c (% enheder) | -0.38 | -1.41** | -0.33 |
| FPG (mg / dL) | 8.8 | -39.2** | -4.5 |
| Vægt (kg) | 3.0 | 2.4*** | -0.90 |
* baseret på intention-to-treat-analyse
** p <0,05 til parvis sammenligning med Prandin og metformin.
*** p <0,05, til parvis sammenligning med metformin.
Et kombinationsbehandlingsregime af Prandin og pioglitazon blev sammenlignet med monoterapi med begge midler alene i en 24-ugers forsøg, der indskrev 246 patienter, der tidligere blev behandlet med sulfonylurinstof eller metformin-monoterapi (HbA1c> 7.0%). Antallet af patienter, der blev behandlet, var: Prandin (N = 61), pioglitazon (N = 62), kombination (N = 123). Prandin-dosis blev titreret i løbet af de første 12 uger, efterfulgt af en 12-ugers vedligeholdelsesperiode. Kombinationsterapi resulterede i signifikant større forbedring af glykæmisk kontrol sammenlignet med monoterapi (figur nedenfor). Ændringerne fra basislinjen for komplementører i FPG (mg / dL) og HbA1c (%) var henholdsvis: -39,8 og -0,1 for Prandin, -35,3 og -0,1 for pioglitazon og -92,4 og -1,9 for kombinationen. I denne undersøgelse, hvor pioglitazondoseringen blev holdt konstant, viste kombinationsbehandlingsgruppen dosisbesparende effekter med hensyn til Prandin (se figurlegenden). Den større effektivitetsrespons for kombinationsgruppen blev opnået ved en lavere daglig repagliniddosis end i Prandin-monoterapigruppen. Gennemsnitlige vægtforøgelser forbundet med kombinationsterapi, Prandin og pioglitazonbehandling var henholdsvis 5,5 kg, 0,3 kg og 2,0 kg.
HbA1c Værdier fra Prandin / Pioglitazon-kombinationundersøgelse

HbA1c værdier pr. studieuge for patienter, der afsluttede studiet (kombination, N = 101; Prandin, N = 35, pioglitazon, N = 26).
Personer med FPG over 270 mg / dL blev trukket ud af undersøgelsen.
Pioglitazondosis: fastlagt til 30 mg / dag; Prandin median slutdosis: 6 mg / dag til kombination og 10 mg / dag til monoterapi.
Et kombinationsbehandlingsregime af Prandin og rosiglitazon blev sammenlignet med monoterapi med begge midler alene i et 24-ugers forsøg, der indgik 252 patienter, der tidligere blev behandlet med sulfonylurinstof eller metformin (HbA1c > 7.0%). Kombinationsterapi resulterede i signifikant større forbedring af glykæmisk kontrol sammenlignet med monoterapi (tabel nedenfor). De glykæmiske virkninger af kombinationsbehandlingen var dosisbesparende med hensyn til både den totale daglige Prandin-dosering og den totale daglige rosiglitazondosering (se tabeloversigten). Et større effektivitetsrespons for kombinationsterapigruppen blev opnået med halvdelen af den gennemsnitlige daglige dosis Prandin og rosiglitazon sammenlignet med de respektive monoterapigrupper. Gennemsnitlig vægtændring forbundet med kombinationsterapi var større end Prandin-monoterapi.
Gennemsnitlige ændringer fra baseline i glykæmiske parametre og vægt i en 24-ugers kombinationundersøgelse af prandin / rosiglitazon *
| Prandin | kombination | Rosiglitazon | |
| N | 63 | 127 | 62 |
| HbA1c (%) | |||
| Baseline | 9.3 | 9.1 | 9.0 |
| Skift med 24 uger | -0.17 | -1.43** | -0.56 |
| FPG (mg / dL) | |||
| Baseline | 269 | 257 | 252 |
| Skift med 24 uger | -54 | -94** | -67 |
| Ændring i vægt (kg) | +1.3 | +4.5*** | +3.3 |
Afsluttende mediandoser: rosiglitazon - 4 mg / dag til kombination og 8 mg / dag til monoterapi; Prandin - 6 mg / dag til kombination og 12 mg / dag til monoterapi |
* baseret på intention-to-treat-analyse
** p-værdi ‰ ¤ 0,001 til sammenligning med begge monoterapi
*** p-værdi <0,001 til sammenligning med Prandin
top
Indikationer og anvendelse
Prandin er indikeret som et supplement til diæt og motion for at forbedre den glykæmiske kontrol hos voksne med type 2-diabetes mellitus.
top
Kontraindikationer
Prandin er kontraindiceret til patienter med:
- Diabetisk ketoacidose, med eller uden koma. Denne tilstand skal behandles med insulin.
- Type 1 diabetes.
- Kendt overfølsomhed over for stoffet eller dets inaktive ingredienser.
top
Forholdsregler
Generel:
Prandin er ikke indiceret til brug i kombination med NPH-insulin (se BIVIRKNINGER, Kardiovaskulære begivenheder)
Makrovaskulære resultater:
Der har ikke været nogen kliniske undersøgelser, der viser, at der foreligger afgørende bevis for reduktion af makrovaskulær risiko med Prandin eller noget andet diabetisk middel.
hypoglykæmi:
Alle orale blodglukosesænkende medikamenter, inklusive repaglinid, er i stand til at producere hypoglykæmi. Korrekt valg af patient, dosering og instruktioner til patienterne er vigtige for at undgå hypoglykæmiske episoder. Nedsat leverfunktion kan forårsage forhøjede repaglinidblodniveauer og kan nedsætte glukoneogen kapacitet, som begge øger risikoen for alvorlig hypoglykæmi. Ældre, svækkede eller underernærede patienter og patienter med binyrer, hypofyse, lever eller svære nyreinsufficiens kan være særligt modtagelig for den hypoglykæmiske virkning af glukosesænkende lægemidler.
Hypoglykæmi kan være vanskeligt at genkende hos ældre og hos personer, der tager beta-adrenerge lægemidler. Det er mere sandsynligt, at hypoglykæmi forekommer, når kaloriindtagelsen er mangelfuld, efter svær eller langvarig træning, når der indtages alkohol, eller når der bruges mere end et glukosesænkende stof.
Hyppigheden af hypoglykæmi er større hos patienter med type 2-diabetes, der ikke tidligere er blevet behandlet med orale blodsukkersænkende medikamenter (nave), eller hvis HbA1c er mindre end 8%. Prandin bør administreres sammen med måltider for at mindske risikoen for hypoglykæmi.
Tab af kontrol med blodsukker:
Når en patient, der stabiliseres på et diabetisk diæt, udsættes for stress, såsom feber, traumer, infektion eller kirurgi, kan et tab af glykæmisk kontrol forekomme. På sådanne tidspunkter kan det være nødvendigt at afbryde Prandin og administrere insulin. Effektiviteten af ethvert hypoglykæmisk lægemiddel til at sænke blodsukkeret til et ønsket niveau falder hos mange patienter over et tidsrum, der kan skyldes udvikling af diabetesens sværhedsgrad eller nedsat lydhørhed over for narkotika. Dette fænomen kaldes sekundær fiasko for at skelne det fra primær svigt, hvor lægemidlet er ineffektivt i en individuel patient, når lægemidlet først gives. Tilstrækkelig justering af dosis og overholdelse af diæt bør vurderes, før en patient klassificeres som en sekundær fiasko.
Oplysninger til patienter
Patienter skal informeres om de potentielle risici og fordele ved Prandin og om alternative behandlingsformer. De bør også informeres om vigtigheden af overholdelse af diætinstruktioner, om et regelmæssigt træningsprogram og om regelmæssig test af blodsukker og HbA1c. Risikoen for hypoglykæmi, dens symptomer og behandling og tilstande, der disponerer for dens udvikling og samtidig administration af andre glukosesænkende lægemidler bør forklares til patienter og ansvarlig familie medlemmer. Primær og sekundær fiasko skal også forklares.
Patienter skal instrueres om at tage Prandin før måltider (2, 3 eller 4 gange om dagen forudgående). Doserne tages normalt inden for 15 minutter efter måltidet, men tiden kan variere fra umiddelbart før måltidet til så længe som 30 minutter før måltidet. Patienter, der springer over et måltid (eller tilsætter et ekstra måltid), skal instrueres om at springe (eller tilføje) en dosis til det måltid.
Laboratorietest
Reaktion på alle diabetiske behandlinger skal overvåges ved periodiske målinger af fastende blod glukose og glycosyleret hæmoglobinniveauer med et mål at sænke disse niveauer mod det normale rækkevidde. Under dosisjustering kan fastende glukose bruges til at bestemme den terapeutiske respons. Derefter skal både glukose og glykosyleret hæmoglobin overvåges. Glykosyleret hæmoglobin kan være særligt nyttigt til evaluering af langvarig glykæmisk kontrol. Postprandial test af glukoseniveau kan være klinisk nyttig hos patienter, hvis blodglukoseniveauer før måltid er tilfredsstillende, men hvis samlede glykæmisk kontrol (HbA1c) er utilstrækkelig.
Drug-Drug Interactions
In vitro-data indikerer, at Prandin metaboliseres af cytochrome P450-enzymer 2C8 og 3A4. Følgelig kan repaglinidmetabolismen ændres af medikamenter, der påvirker disse cytochrome P450-enzymsystemer via induktion og inhibering. Der skal derfor udvises forsigtighed hos patienter, der er på Prandin og tager hæmmere og / eller inducerende CYP2C8 og CYP3A4. Virkningen kan være meget signifikant, hvis begge enzymer hæmmes på samme tid, hvilket resulterer i en markant stigning i plasmakoncentrationer af repaglinid. Lægemidler, der vides at hæmme CYP3A4, inkluderer antifungale midler som ketoconazol, itraconazol og antibakterielle midler som erythromycin. Lægemidler, der vides at hæmme CYP2C8, inkluderer midler som trimethoprim, gemfibrozil og montelukast. Lægemidler, der inducerer CYP3A4- og / eller 2C8-enzymsystemerne inkluderer rifampin, barbiturater og carbamezapin. Se KLINISK FARMAKOLOGI afsnit, Drug-Drug Interactions.
In vivo-data fra en undersøgelse, der evaluerede samtidig indgivelse af et cytochrome P450-enzym 3A4 inhibitor, klarithromycin, med Prandin resulterede i en klinisk signifikant stigning i repaglinid plasmaniveauer. Derudover blev der observeret en stigning i repaglinidplasmaniveauer i en undersøgelse, der vurderede samtidig indgivelse af Prandin med trimethoprim, en cytochrome P-450-enzym 2C8-hæmmer. Disse stigninger i repaglinidplasmaniveauer kan muliggøre en justering af Prandin-dosis. Se KLINISK FARMAKOLOGIafsnit, Drug-Drug Interactions.
In vivo-data fra en undersøgelse, der evaluerede samtidig administration af gemfibrozil og Prandin hos raske forsøgspersoner resulterede i en signifikant stigning i repaglinidblodniveauer. Patienter, der tager Prandin, bør ikke begynde at tage gemfibrozil; patienter, der tager gemfibrozil, bør ikke begynde at tage Prandin. Samtidig brug kan resultere i forbedrede og langvarige blodsukkersænkende virkninger af repaglinid. Der skal udvises forsigtighed hos patienter, der allerede er i Prandin og gemfibrozil - blodglukoseniveauer skal overvåges, og Prandin-dosisjustering kan være nødvendig. Sjældne hændelser efter markedsføring af alvorlig hypoglykæmi er rapporteret hos patienter, der tager Prandin og gemfibrozil sammen. Gemfibrozil og itraconazol havde en synergistisk metabolisk inhiberende effekt på Prandin. Derfor bør patienter, der tager Prandin og gemfibrozil, ikke tage itraconazol. Se KLINISK FARMAKOLOGI afsnit, Drug-Drug Interactions.
Den hypoglykæmiske virkning af orale blodglukosesænkende midler kan potentieres af visse lægemidler, herunder ikke-steroide antiinflammatoriske midler og andre lægemidler. der er stærkt proteinbundne, salicylater, sulfonamider, chloramphenicol, coumariner, probenecid, monoaminoxidaseinhibitorer og beta-adrenerg blokering midler. Når sådanne lægemidler administreres til en patient, der modtager orale blodsukkersænkende midler, skal patienten følges nøje for hypoglykæmi. Når sådanne lægemidler trækkes tilbage fra en patient, der får orale blodglukosesænkende midler, skal patienten følges nøje for tab af glykæmisk kontrol.
Visse lægemidler har en tendens til at producere hyperglykæmi og kan føre til tab af glykæmisk kontrol. Disse lægemidler inkluderer thiazider og andre diuretika, kortikosteroider, phenothiaziner, skjoldbruskkirtelprodukter, østrogener, orale prævention, phenytoin, nicotinsyre, sympatomimetika, calciumkanalblokerende medikamenter, og isoniazid. Når disse lægemidler administreres til en patient, der får orale blodsukkersænkende midler, skal patienten observeres for tab af glykæmisk kontrol. Når disse lægemidler trækkes tilbage fra en patient, der får orale blodsukkersænkende midler, skal patienten følges nøje for hypoglykæmi.
Karcinogenese, mutagenese og forringelse af fertilitet
Langvarige carcinogenicitetsundersøgelser blev udført i 104 uger i doser op til og med 120 mg / kg kropsvægt / dag (rotter) og 500 mg / kg kropsvægt / dag (mus) eller henholdsvis ca. 60 og 125 gange klinisk eksponering for en mg / m2 basis. Der blev ikke fundet noget bevis for kræftfremkaldende virkning hos mus eller hunrotter. Hos hanrotter var der en øget forekomst af godartede adenomer i skjoldbruskkirtlen og leveren. Relevansen af disse fund for mennesker er uklar. Ingen-virkningsdoserne for disse observationer hos hanrotter var 30 mg / kg legemsvægt / dag for skjoldbruskkirtel tumorer og 60 mg / kg kropsvægt / dag for leversvulster, der er henholdsvis over 15 og 30 gange klinisk eksponering på en mg / m2 basis.
Repaglinid var ikke-genotoksisk i et batteri in vivo og in vitro-studier: Bakteriel mutagenese (Ames-test), in vitro-fremadcellemutationsassay i V79-celler (HGPRT), in vitro kromosomal aberreringsassay i humane lymfocytter, ikke planlagt og replikerende DNA-syntese i rottelever og in vivo mus- og rotte-mikronukleus tests.
Fertiliteten af han- og hunrotter blev ikke påvirket af repaglinidadministration i doser op til 80 mg / kg legemsvægt / dag (hunner) og 300 mg / kg legemsvægt / dag (hanner); over 40 gange klinisk eksponering på mg / m2-basis.
Graviditet
Graviditet kategori C
Teratogene virkninger
Sikkerhed hos gravide er ikke fastlagt. Repaglinid var ikke teratogent hos rotter eller kaniner i doser 40 gange (rotter) og ca. 0,8 gange (kanin) klinisk eksponering (på mg / m2 basis) under hele graviditeten. Da dyrefortplantningsundersøgelser ikke altid er forudsigelige for menneskelig respons, bør Prandin kun bruges under graviditet, hvis det er klart nødvendigt.
Fordi nylige oplysninger antyder, at unormale blodsukkerniveauer under graviditet er forbundet med en højere forekomst af medfødte abnormiteter, anbefaler mange eksperter, at insulin bruges under graviditet til at opretholde blodsukkerniveauet så tæt på det normale som muligt.
Ikke-teratogene virkninger
Afkom af rottedammer udsat for repaglinid ved 15 gange klinisk eksponering på mg / m2-basis i dag 17 til 22 i drægtighedsperioden og under amning udviklede ikke-teratogene skeletdeformiteter bestående af forkortelse, fortykning og bøjning af humerus i løbet af den postnatale periode. Denne virkning blev ikke set ved doser op til 2,5 gange klinisk eksponering (på mg / m2-basis) på dagene 1 til 22 af graviditeten eller ved højere doser givet i dagene 1 til 16 af graviditeten. Relevant menneskelig eksponering er ikke hidtil forekommet, og sikkerheden ved administration af Prandin under graviditet eller amning kan derfor ikke fastlægges.
Sygeplejerske mødre
I reproduktionsundersøgelser hos rotter blev der målt målbare niveauer af repaglinid i modermælkenes modermælk, og der blev observeret nedsatte blodglukoseniveauer hos hvalpene. Krydsfremmende undersøgelser indikerede, at skeletændringer (se ikke-teratogene virkninger ovenfor) kunne induceres i kontrollere hvalpe, der ammes af behandlede dæmninger, skønt dette forekom i mindre grad end dem, der blev behandlet i livmoderen. Selvom det ikke vides, om repaglinid udskilles i modermælk, vides det, at nogle orale stoffer udskilles på denne måde. Fordi potentialet for hypoglykæmi hos ammende spædbørn kan eksistere, og på grund af virkningen på ammende dyr, a der skal træffes beslutning om, hvorvidt Prandin skal seponeres hos ammende mødre, eller om mødre skal ophøre ammende. Hvis Prandin seponeres, og hvis diæt alene ikke er tilstrækkelig til at kontrollere blodsukkeret, bør insulinbehandling overvejes.
Pædiatrisk brug
Der er ikke udført undersøgelser hos pædiatriske patienter.
Geriatrisk brug
I kliniske repaglinidundersøgelser på 24 uger eller mere var 415 patienter over 65 år. I et år, aktivt kontrollerede studier, blev der ikke set forskelle i effektivitet eller bivirkninger mellem disse forsøgspersoner og de mindre end 65 andre end den forventede aldersrelaterede stigning i hjerte-kar-hændelser observeret for Prandin og komparator lægemidler. Der var ingen stigning i hyppighed eller sværhedsgrad af hypoglykæmi hos ældre. Anden rapporteret klinisk erfaring har ikke identificeret forskelle i svar mellem ældre og yngre patienter, men større følsomhed hos nogle ældre individer for Prandin-terapi kan ikke bestemmes ud.
top
Bivirkninger
Hypoglykæmi: Se FORHOLDSREGLER ogOVERDOSERING sektioner.
Prandin er blevet administreret til 2931 individer under kliniske forsøg. Cirka 1500 af disse personer med type 2-diabetes er blevet behandlet i mindst 3 måneder, 1000 i mindst 6 måneder og 800 i mindst 1 år. Størstedelen af disse individer (1228) modtog Prandin i en af fem 1-årige, aktiv-kontrollerede forsøg. Sammenligningsmedicinene i disse 1-årige forsøg var orale sulfonylurinstof (SU) inklusive glyburid og glipizid. I løbet af et år blev 13% af Prandin-patienterne afbrudt på grund af bivirkninger, ligesom 14% af SU-patienterne. De mest almindelige bivirkninger, der førte til abstinens, var hyperglykæmi, hypoglykæmi og relaterede symptomer (se FORHOLDSREGLER). Mild eller moderat hypoglykæmi forekom hos 16% af Prandin-patienter, 20% af glyburidpatienter og 19% af glipizidpatienter.
Tabellen nedenfor viser almindelige bivirkninger for Prandin-patienter sammenlignet med både placebo (i forsøg på 12 til 24 uger) og med glyburid og glipizid i et års forsøg. Prandins bivirkningsprofil var generelt sammenlignelig med profilen for sulfonylurinstof (SU).
Almindeligt rapporterede bivirkninger (% af patienterne) *
| BEGIVENHED | Prandin |
PLACEBO | Prandin |
SU |
| N = 352 | N = 108 | N = 1228 | N = 498 | |
| Placebo-kontrollerede studier | Aktive kontrollerede studier | |||
| Metabolisk | ||||
| hypoglykæmi | 31** | 7 | 16 | 20 |
| Respiratory | ||||
| URI | 16 | 8 | 10 | 10 |
| Bihulebetændelse | 6 | 2 | 3 | 4 |
| Rhinitis | 3 | 3 | 7 | 8 |
| bronkitis | 2 | 1 | 6 | 7 |
| Mave | ||||
| Kvalme | 5 | 5 | 3 | 2 |
| Diarré | 5 | 2 | 4 | 6 |
| Forstoppelse | 3 | 2 | 2 | 3 |
| Opkastning | 3 | 3 | 2 | 1 |
| Dyspepsi | 2 | 2 | 4 | 2 |
| Muskuloskeletal | ||||
| ledsmerter | 6 | 3 | 3 | 4 |
| Rygsmerte | 5 | 4 | 6 | 7 |
| Andet | ||||
| Hovedpine | 11 | 10 | 9 | 8 |
| Parestesi | 3 | 3 | 2 | 1 |
| Brystsmerter | 3 | 1 | 2 | 1 |
| Urinvejsinfektion | 2 | 1 | 3 | 3 |
| Tandeforstyrrelse | 2 | 0 | <1 | <1 |
| Allergi | 2 | 0 | 1 | <1 |
* Begivenheder â 2 ¥ for Prandin-gruppen i de placebokontrollerede studier og â ¥ begivenheder i placebogruppen
** Se prøvebeskrivelse i KLINISK FARMAKOLOGI, Kliniske forsøg.
Kardiovaskulære begivenheder
I et års forsøg, hvor Prandin blev sammenlignet med sulfonylurinstof, var forekomsten af angina sammenlignelig (1,8%) for begge behandlinger med en forekomst af brystsmerter på 1,8% for Prandin og 1,0% for sulfonylurinstoffer. Forekomsten af andre valgte kardiovaskulære hændelser (hypertension, unormal EKG, myokardie) infarkt, arytmier og hjertebanken) var 1 1% og ikke forskellig mellem Prandin og komparator medicin.
Hyppigheden af samlede alvorlige kardiovaskulære bivirkninger, inklusive iskæmi, var højere for repaglinid (4%) end for sulfonylurinstof (3%) i kontrollerede komparative kliniske forsøg. I 1-årige kontrollerede forsøg var Prandin-behandling ikke forbundet med overdreven dødelighed sammenlignet med de observerede satser med andre orale hypoglykæmiske lægemidler.
Oversigt over alvorlige kardiovaskulære hændelser (% af de samlede patienter med hændelser) i forsøg, der sammenligner Prandin med Sulfonylurea
| Prandin | SU | |
| I alt eksponeret | 1228 | 498 |
| Alvorlige CV-begivenheder | 4% | 3% |
| Hjerteisikæmiske begivenheder | 2% | 2% |
| Dødsfald på grund af CV-begivenheder | 0.5% | 0.4% |
* glyburid og glipizid
Syv kontrollerede kliniske forsøg inkluderede Prandin-kombinationsterapi med NPH-insulin (n = 431), insulin formuleringer alene (n = 388) eller andre kombinationer (sulfonylurinstof plus NPH-insulin eller Prandin plus metformin) (N = 120). Der var seks alvorlige bivirkninger af myokardisk iskæmi hos patienter behandlet med Prandin plus NPH-insulin fra to undersøgelser og en hændelse hos patienter, der bruger insulinformuleringer alene fra en anden undersøgelse.
Sjældne bivirkninger (<1% af patienterne)
Mindre almindelige bivirkninger, kliniske eller laboratoriebegivenheder, der blev observeret i kliniske forsøg, omfattede forhøjede leverenzymer, trombocytopeni, leukopeni og anafylaktoide reaktioner.
Selvom der ikke er konstateret nogen årsagsforhold til repaglinid, inkluderer erfaringerne efter markedsføring rapporter om følgende sjældne bivirkninger: alopecia, hæmolytisk anæmi, pancreatitis, Stevens-Johnson syndrom og alvorlig leverdysfunktion inklusive gulsot og hepatitis.
Kombinationsterapi med Thiazolidinedioner
I løbet af 24 ugers behandling kliniske forsøg med Prandin-rosiglitazon eller Prandin-pioglitazon kombinationsterapi (i alt 250 patienter i kombinationsterapi), hypoglykæmi (blodglukose <50 mg / dL) forekom hos 7% af patienter med kombinationsterapi i sammenligning med 7% for monoterapi med Prandin og 2% for thiazolidinedion monoterapi.
Perifert ødem blev rapporteret hos 12 ud af 250 patienter med kombinationsterapi af Prandin-thiazolidinedione og 3 ud af 124 patienter med monoterapi med thiazolidinedione, og ingen tilfælde blev rapporteret i disse forsøg med Prandin monoterapi. Når det korrigeres for frafaldet af behandlingsgrupperne, er procentdelen af patienter, der har hændelser med perifert ødem pr. 24 ugers behandling var 5% for kombinationsterapi af Prandin-thiazolidinedione og 4% for thiazolidinedione monoterapi. Der blev rapporteret hos 2 af 250 patienter (0,8%) behandlet med Prandin-thiazolidinedione-behandling af episoder med ødemer med kongestiv hjertesvigt. Begge patienter havde en tidligere historie med koronararteriesygdom og blev frisk efter behandling med vanddrivende stoffer. Der blev ikke rapporteret sammenlignelige tilfælde i monoterapibehandlingsgrupperne.
Den gennemsnitlige ændring i vægt fra basislinien var +4,9 kg til Prandin-thiazolidinedion-terapi. Der var ingen patienter i kombinationsterapi med Prandin-thiazolidinedione, der havde forhøjelser af levertransaminaser (defineret som 3 gange den øvre grænse for normale niveauer).
top
Overdosis
I et klinisk forsøg modtog patienter stigende doser Prandin op til 80 mg dagligt i 14 dage. Der var få bivirkninger andre end dem, der var forbundet med den tilsigtede virkning af sænkning af blodsukker. Hypoglykæmi forekom ikke, når måltiderne blev givet med disse høje doser. Hypoglykæmiske symptomer uden tab af bevidsthed eller neurologiske fund bør behandles aggressivt med oral glukose og justeringer i lægemiddeldosering og / eller måltidsmønstre. En tæt overvågning kan fortsætte, indtil lægen er sikker på, at patienten er ude af fare. Patienter skal overvåges nøje i mindst 24 til 48 timer, da hypoglykæmi kan gentage sig efter åbenbar klinisk bedring. Der er ingen holdepunkter for, at repaglinid kan dialyseres ved hjælp af hæmodialyse.
Alvorlige hypoglykæmiske reaktioner med koma, anfald eller anden neurologisk svækkelse forekommer sjældent, men udgør medicinske nødsituationer, der kræver øjeblikkelig hospitalisering. Hvis hypoglykæmisk koma er diagnosticeret eller mistænkes, skal patienten gives en hurtig intravenøs injektion af koncentreret (50%) glukoseopløsning. Dette skal efterfølges af en kontinuerlig infusion af mere fortyndet (10%) glukoseopløsning med en hastighed, der opretholder blodglukosen på et niveau over 100 mg / dL.
top
Dosering og administration
Der er ingen fast doseringsregime til behandling af type 2-diabetes med Prandin.
Patientens blodsukker bør overvåges regelmæssigt for at bestemme den minimale effektive dosis for patienten; at detektere primær fiasko, dvs. utilstrækkelig sænkning af blodsukker ved den maksimale anbefalede dosis af medicin; og til at detektere sekundær fiasko, dvs. tab af en passende blodsukkersænkende respons efter en indledende effektivitetsperiode. Glykosylerede hæmoglobinniveauer er af værdi ved overvågning af patientens længerevarende respons på terapi.
Kortvarig administration af Prandin kan være tilstrækkelig i perioder med kortvarigt tab af kontrol hos patienter, der normalt er godt kontrolleret i kosten.
Prandin-doser tages normalt inden for 15 minutter efter måltidet, men tiden kan variere fra umiddelbart før måltidet til så længe som 30 minutter før måltidet.
Startdosis
For patienter, der ikke tidligere er behandlet, eller hvis HbA1c er <8%, skal startdosis være 0,5 mg for hvert måltid. For patienter, der tidligere er behandlet med blodsukkersænkende medikamenter, og hvis HbA1c er â € ¥ 8%, er den indledende dosis 1 eller 2 mg med hvert måltid forudgående (se forrige afsnit).
Dosisjustering
Dosisjusteringer skal bestemmes ved blodglukoserespons, normalt fastende blodsukker. Test af postprandial glukoseniveau kan være klinisk nyttig hos patienter, hvis blodglukoseniveau før måltid er tilfredsstillende, men hvis samlede glykæmisk kontrol (HbA1c) er utilstrækkelig. Den prærandielle dosis skal fordobles op til 4 mg med hvert måltid, indtil der opnås tilfredsstillende blodglukoserespons. Der skal gå mindst en uge for at vurdere respons efter hver dosisjustering.
Det anbefalede dosisområde er 0,5 mg til 4 mg taget med måltider. Prandin kan doseres preprandialt 2, 3 eller 4 gange om dagen som respons på ændringer i patientens måltidsmønster. Den maksimale anbefalede daglige dosis er 16 mg.
Patientstyring
Langvarig effekt skal overvåges ved måling af HbA1c-niveauer ca. hver 3. måned. Manglende overholdelse af et passende doseringsregime kan udfælde hypoglykæmi eller hyperglykæmi. Patienter, der ikke overholder deres ordinerede diæt- og medikamentregime, er mere tilbøjelige til at udvise utilfredsstillende respons på terapi, herunder hypoglykæmi. Når der forekommer hypoglykæmi hos patienter, der tager en kombination af Prandin og en thiazolidinedion eller Prandin og metformin, bør Prandin-dosis reduceres.
Patienter, der modtager andre orale hypoglykæmiske midler
Når Prandin bruges til at erstatte behandling med andre orale hypoglykæmiske midler, kan Prandin startes dagen efter, at den endelige dosis er givet. Patienter skal derefter observeres omhyggeligt for hypoglykæmi på grund af potentiel overlapning af lægemiddeleffekter. Når det overføres fra længere halveringstid af sulfonylurinstoffer (f.eks. Chlorpropamid) til repaglinid, kan tæt monitorering indikeres i op til en uge eller længere.
Kombinationsterapi
Hvis Prandin monoterapi ikke resulterer i tilstrækkelig glykæmisk kontrol, kan metformin eller en thiazolidinedion tilføjes. Hvis metformin eller thiazolidinedione monoterapi ikke giver tilstrækkelig kontrol, kan Prandin tilføjes. Startdosis og dosisjusteringer til Prandin-kombinationsterapi er de samme som for Prandin-monoterapi. Dosis af hvert lægemiddel skal justeres omhyggeligt for at bestemme den minimale dosis, der kræves for at opnå den ønskede farmakologiske virkning. Undladelse af at gøre dette kan resultere i en stigning i forekomsten af hypoglykæmiske episoder. Passende overvågning af FPG- og HbA1c-målinger bør bruges for at sikre, at patienten ikke udsættes for overdreven medicineksponering eller øget sandsynlighed for sekundær lægemiddelsvigt.
top
Hvordan leveres
Prandin (repaglinid) tabletter leveres som uskårede, bikonvekse tabletter, der fås i 0,5 mg (hvid), 1 mg (gul) og 2 mg (fersken) styrke. Tabletter er præget af Novo Nordisk (Apis) tyresymbol og farvet for at indikere styrke.
| 0,5 mg tabletter (hvide) | Flasker på 100 | NDC 00169-0081-81 |
| Flasker på 500 | NDC 00169-0081-82 | |
| Flasker på 1000 | NDC 00169-0081-83 | |
| 1 mg tabletter (gul) | Flasker på 100 | NDC 00169-0082-81 |
| Flasker på 500 | NDC 00169-0082-82 | |
| Flasker på 1000 | NDC 00169-0082-83 | |
| 2 mg tabletter (fersken) | Flasker på 100 | NDC 00169-0084-81 |
| Flasker på 500 | NDC 00169-0084-82 | |
| Flasker på 1000 | NDC 00169-0084-83 |
Opbevar ikke over 25 ° C.
Beskyt mod fugt. Hold flasker tæt lukket.
Dispenser i tætte containere med sikkerhedslukker.
Licenseret under US patent nr. RE 37,035.
Prandin® er et registreret varemærke tilhørende Novo Nordisk A / S.
Fremstillet i Tyskland til
Novo Nordisk Inc.
Princeton, NJ 08540
1-800-727-6500
www.novonordisk-us.com
© 2003-2008 Novo Nordisk A / S
Prandin, patientinformation (på almindeligt engelsk)
Detaljeret information om tegn, symptomer, årsager, behandling af diabetes
sidst opdateret 06/2009
Oplysningerne i denne monografi er ikke beregnet til at dække alle mulige anvendelser, instruktioner, forholdsregler, medikamentinteraktion eller ugunstige virkninger. Denne information er generaliseret og er ikke beregnet til specifik medicinsk rådgivning. Hvis du har spørgsmål til de lægemidler, du tager eller ønsker flere oplysninger, skal du kontakte din læge, apotek eller sygeplejerske.
tilbage til: Gennemse alle medicin mod diabetes



